Nội dung bài viết
MgSO4 – Magiê sunfat là một loại muối vô cơ, chứa magie, lưu huỳnh và oxy. Nó tồn tại trong tự nhiên dưới dạng tinh thể màu trắng, dễ hòa tan trong nước. Trong bài viết này, hãy cùng Vietchem tìm hiểu chi tiết về đặc tính, tính chất của MgSO4.
1. MgSO4 hóa học là gì?
Định nghĩa: MgSO4 là muối vô cơ bao gồm magie, oxy và lưu huỳnh. Trong tự nhiên, nó được tìm thấy dưới dạng tinh thể màu trắng, có vị đắng, mùi đặc trưng và dễ hòa tan.
Ảnh 1: Công thức phân tử của MgSO4
Tên gọi khác: MgSO4 còn có tên gọi khác như: Magie sunfat, muối Epsom (heptahydrat), muối Anh, muối đắng
Cấu trúc hóa học của nó như sau:
Khối lượng nguyên tử của MgSO4 là: 120,366g/mol
Số oxi hóa của MgSO4: -2
2. Tính chất vật lý của MgSO4
- Nó là một hợp chất rắn, kết tinh có vị đắng.
- MgSO4 có màu gì: Trắng
- MgSO4 dễ dàng hút ẩm từ không khí, hòa tan trong nước và một số dung môi khác nhau như rượu, glycerol nhưng không tan trong axeton.
- Trọng lượng riêng của muối này: 2,66 g/cm3
- Khi ở dạng khan, MgSO4 phân hủy ở nhiệt độ 1124 độ C.
- Ở dạng muối Epsom, MgSO4 phân hủy ở nhiệt độ 150 độ C.
- Độ hòa tan trong nước của MgSO4 là 26,9 g/100 ml. Tùy thuộc vào nhiệt độ và dạng tinh thể, độ hòa tan sẽ thay đổi.

Ảnh 2: MgSO4 ở dạng tinh thể rắn, màu trắng
MgSO4 có kết tủa không? Magie sunfat không phải là chất kết tủa. Nhưng nếu chúng ta phản ứng với dung dịch bazơ, chúng ta sẽ thu được kết tủa:
Ví dụ: MgSO4 + 2NaOH → Mg(OH)2↓ + Na2SO4.
3. Tính chất hóa học của MgSO4
Chúng ta sẽ tìm hiểu chi tiết về tính chất hóa học của Magiê sunfat thông qua các phản ứng hóa học sau đây.
3.1. MgSO4 phản ứng với NaOH
Phản ứng hóa học: MgSO4 + NaOH = Mg(OH)2 + Na2SO4
Phản ứng này có thể xảy ra ở điều kiện bình thường. Kết tủa trắng xuất hiện trong dung dịch là Mg(OH)2.
3.2. Phản ứng MgSO4 + HCl
Phản ứng này không xảy ra. Nguyên nhân là muối có thể phản ứng với axit nếu tạo thành kết tủa. Đặc biệt, axit tạo thành phải mạnh hơn axit tham gia phản ứng.
3.3. Phản ứng với kim loại (MgSO4 + Fe)
Phương trình phản ứng: Fe + MgSO4 → Mg + FeSO4
Đây là phản ứng trao đổi trong đó các nguyên tử kim loại trao đổi vị trí với nhau. Từ đó, muối mới được hình thành.
3.4. Phản ứng Al + MgSO4
Không có phản ứng nào xảy ra vì Mg có hoạt tính hóa học mạnh hơn Al. Vậy Al không thể đẩy Mg ra khỏi muối của nó.
3.5. Phản ứng Ba + MgSO4
Các phương trình phản ứng xảy ra:
- Ba + 2H2O = Ba(OH)2 + H2
- MgSO4 + Ba(OH)2 = BaSO4 + Mg(OH)2
Lúc này sẽ xuất hiện hai loại kết tủa là BaSO4 và Mg(OH)2, đều có màu trắng.
3.6. MgSO4 phản ứng với nước
Phương trình: MgSO4 + 7H2O → MgSO4(H2O)7
Như đã đề cập, MgSO4 có thể dễ dàng hòa tan trong nước. Trong điều kiện bình thường, phản ứng tổng hợp này xảy ra với sản phẩm muối heptahydrat magie sunfat.
3.7. MgSO4 phản ứng với KOH
Phương trình hóa học: MgSO4 + 2KOH → Mg(OH)2 ↓ + K2SO4
Phản ứng này xảy ra khi cho từ từ KOH vào dung dịch muối MgSO4. Lúc này thu được kết tủa trắng chính là Mg(OH)2.
3.8. NH3 phản ứng với MgSO4
Phương trình hóa học: MgSO4 + 2NH3 + 2H2O → Mg(OH)2 + (NH4)2SO4
Đây là phản ứng trao đổi Nó tạo thành sản phẩm chính là muối amoni sunfat. Điều kiện để xảy ra phản ứng là phải có dung dịch. Sau phản ứng sẽ thu được kết tủa Mg(OH)2.
3.9. Phản ứng MgSO4 tạo ra Mg
Phương trình hóa học: MgSO4 → Mg + SO4
Đây là phản ứng phân hủy, phản ứng oxi hóa khử. Ở đó, MgSO4 phân hủy tạo thành kim loại magie và SO4.
4. Magie sunfat có tác dụng gì?
4.1. Tác dụng của MgSO4 đối với cây trồng
Trong ngành nông nghiệp, MgSO4 được sử dụng rất nhiều trong việc tạo ra phân bón Magie. Từ đó, đảm bảo cung cấp đủ magie, mang lại cho cây trồng những lợi ích sau:
- Có lá xanh tươi, quang hợp tốt, không rụng lá.
- Thúc đẩy tổng hợp chất dinh dưỡng và tăng sức đề kháng cho cây trồng.
- Ngăn chặn đất trống trở nên cứng.
- Giúp cây phát triển nhanh hơn.
- Magiê là chất trung hòa đất, giúp cây trồng phát triển tốt nhất.
4.2. MgSO4 và ứng dụng trong y học
Cơ chế tác động của MgSO4 lên ruột đã được đề cập từ lâu. Nó giúp tăng thể tích phân bằng cách giữ lại chất lỏng trong lòng ruột. Kéo dài ruột và tăng nhu động ruột. Vì vậy, MgSO4 sẽ hỗ trợ nhuận tràng.
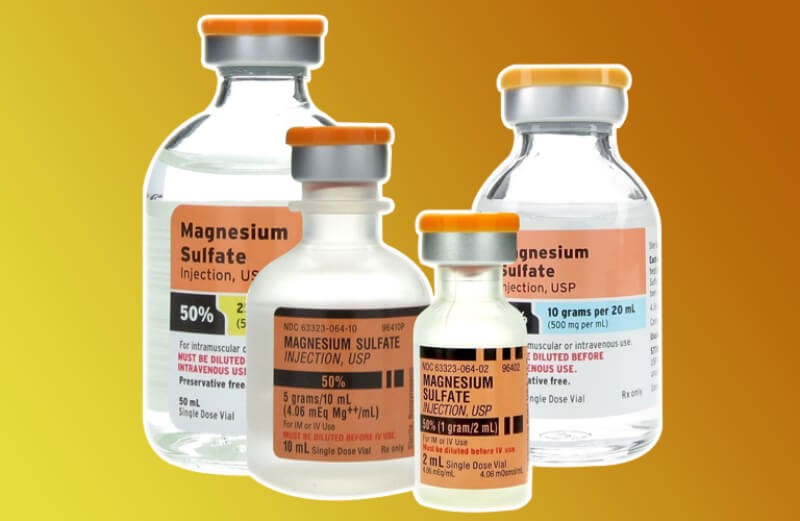
Ảnh 3: MgSO4 là hoạt chất không thể thiếu trong y học
Ngoài ra, nó còn có những tác dụng sau trong y học:
- Magie là thành phần quan trọng cần được bổ sung liên tục cho cơ thể.
- Dùng MgSO4 làm dịu cơn đau cơ
- Điều trị bệnh động kinh bằng cách giảm các xung thần kinh.
4.3. Ứng dụng MgSO4 trong các ngành công nghiệp khác
- Quy trình xử lý nước và in nhuộm vải
- Sản xuất thức ăn chăn nuôi, nâng cao chất lượng thịt
- Làm trắng bột giấy
- Tăng mức độ màu của mực
- Tăng cường độ chống đông của bê tông
- Sử dụng làm chất keo tụ trong làm đậu phụ thủ công
- Được sử dụng trong muối tắm.
4.4. Ứng dụng MgSO4 trong phòng thí nghiệm
Nó được coi là một chất làm khô tổng hợp hữu cơ. Nguyên nhân là do các nhà khoa học lợi dụng ái lực của nó với nước.
5. Những câu hỏi thường gặp về MgSO4
Để nhận biết HCl, NaOH, MgSO4 người ta dùng phương pháp nào?
Dùng quỳ tím. HCl làm quỳ tím chuyển sang màu đỏ, NaOH làm quỳ tím chuyển sang màu xanh, MgSO4 không đổi màu.
MgSO4 có tan trong nước không?
MgSO4 tan nhiều trong nước.
MgSO4 là chất điện li mạnh hay yếu?
MgSO4 là một trong những chất điện li mạnh.
MgSO4 là muối gì?
MgSO4 là muối epsom, dạng hexahydrat.
MgSO4 làm quỳ tím chuyển sang màu gì?
Hóa chất này không làm đổi màu quỳ tím.
Như vậy, Vietchem đã giúp bạn tìm hiểu chi tiết về muối MgSO4. Hy vọng thông tin này hữu ích cho bạn. Nếu bạn có nhu cầu mua hoặc tìm hiểu về hóa chất hãy liên hệ ngay với Vietchem để được tư vấn.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn