Nội dung bài viết
HClO được sử dụng rất nhiều trong việc vệ sinh bể bơi để giữ cho bể bơi luôn trong xanh, sạch sẽ. Vậy HClO là gì? Tính chất và ứng dụng của HClO? Thông tin chi tiết sẽ được Trường Chu Văn An giải đáp dưới đây, chúng ta cùng nhau tìm hiểu nhé.
1. HClO là gì?
HClO là axit hypochlorous và có nhiều tên gọi khác như: Chlorine Hydroxide, Hydrogen Hypochlorite. Đây là axit yếu có tác dụng khử trùng tốt nên được dùng để làm sạch bể bơi và một số ngành công nghiệp khác.
Công thức phân tử của HClO
2. Tính chất hóa lý của HClO
2.1. Tính chất vật lý
Axit hypochlorous có độ pH 7,53 và trọng lượng phân tử 52,46g/mol. Trong điều kiện bình thường, HClO tồn tại ở dạng lỏng và dễ hòa tan trong nước.
HClO là axit yếu nên dễ phân ly thành axit hypoclorơ. Khi đó Axit hypoclorơ tồn tại ở trạng thái oxi hóa +1. Tuy nhiên, chất này lại là tác nhân oxy hóa mạnh vì khi tiếp xúc với một số chất khác có thể gây nổ hóa học.
2.2. Tính chất hóa học
Axit hypochlorous sở hữu các tính chất hóa học độc đáo. Bao gồm:
Thể hiện tính chất oxy hóa mạnh
Phản ứng thu được khí clo có phương trình phản ứng:
2HClO + 2H+ + 2e- ⇔ Cl2 + 2H2O
Axit hypoclorơ tác dụng với axit clohiđric
Sau khi phản ứng kết thúc thu được khí clo có phương trình phản ứng:
HClO + HCl → H2O +Cl2
Tham gia vào quá trình phân chia
HClO ở dạng Hypochlorite Anion sẽ phản ứng ngay cả khi ở trạng thái ngậm nước hoặc dung dịch. Đây là phản ứng hai chiều có phương trình:
HClO ⇔ OCl- + H+
Ngoài ra muối HClO còn được dùng làm chất tẩy rửa. Chúng có công thức phân tử NaClO và được gọi là Hypochlorite.
3. Điều chế axit hypoclorơ
Có nhiều cách điều chế Axit hypoclorơ tùy theo mục đích và quy mô sử dụng. Cụ thể:
Điều chế bằng cách cho Kali hypoclorit phản ứng với nước:
Theo phương trình phản ứng: H2O + KClO → KHCO3 + HClO
Được điều chế bằng cách tạo bọt khí clo trong nước:
Phương trình phản ứng như sau: Cl2 + H2O ⇔ HClO + HCl
Điều chế bằng cách cho Ca(ClO)2 phản ứng với nước và xúc tác CO2:
Phương trình phản ứng: H2O + Ca(ClO)2 → CaCO3 (kết tủa) + HClO
4. Ứng dụng của axit hypoclorơ
HClO được sử dụng khá phổ biến trong đời sống nhưng được biết đến nhiều nhất với công dụng khử trùng và tẩy trắng. Đặc biệt là khử trùng bể bơi và xử lý nước thải.
HClO trong công nghiệp thực phẩm có vai trò vô cùng quan trọng. Nguyên liệu này được sử dụng trong khâu làm sạch trước khi chế biến thực phẩm. Nhờ đặc tính an toàn nên chúng không gây hại cho sức khỏe con người.
Ngoài ra, HClO là một phần của quá trình chuyển đổi Hydrochloric Clorua từ Anken.

Ứng dụng HClO trong xử lý nước
5. Tính chất điện phân của HClO
Axit HClO là chất điện li yếu. Vì khi hòa tan chỉ có một số ít phân tử phân ly thành ion. Các phân tử còn lại không phân ly mà tồn tại trong dung dịch ở dạng phân tử ban đầu.
Trong trường hợp điện phân, chúng sẽ dễ dàng phân hủy tạo thành các Anion Hypochlorite bao gồm H+ và Cl-. Phương trình: HClO ⇆ H+ + ClO−
Trong khi đó, muối gốc ClO- có đặc tính làm sạch và khử trùng tốt. Vì vậy, chúng được sử dụng rộng rãi trong lĩnh vực thực phẩm, hóa chất, làm sạch…
6. Tác hại của HClO đối với sức khỏe
Dù được sử dụng rộng rãi trên thị trường trong nhiều lĩnh vực khác nhau nhưng dung dịch HClO có thể gây hại cho sức khỏe con người. Đây là hợp chất oxy hóa mạnh nên khi tiếp xúc trực tiếp với cơ thể sẽ gây viêm, kích ứng hoặc các tổn thương khác.
HClO tiềm ẩn nhiều mối nguy hiểm nên sau khi tiếp xúc cần phải xử lý đúng cách để tránh ảnh hưởng xấu đến sức khỏe. Các biện pháp cụ thể như sau:
6.1. Hít phải HClO
Khi hít phải khí HClO, người ta có thể gặp các vấn đề như: Viêm phổi, ho, nghẹt mũi, khó thở. Nếu xuất hiện những dấu hiệu trên, hãy nhanh chóng chạy ra khỏi nơi bị nhiễm Axit Hypochlorous để hít thở không khí trong lành. Trường hợp khó thở cần can thiệp bằng máy thở và đến cơ sở y tế gần nhất để được cấp cứu kịp thời.
6.2. Nuốt phải axit hypochlorous
Nếu nuốt phải, axit hypochlorous có thể gây đau, loét dạ dày, nôn ra máu, đau họng hoặc buồn nôn. Trong trường hợp này, hãy cố gắng hạn chế nôn mửa và uống nhiều nước để làm loãng nồng độ HClO. Tuyệt đối không uống bất kỳ loại sữa hay đồ uống có ga, cồn nào.
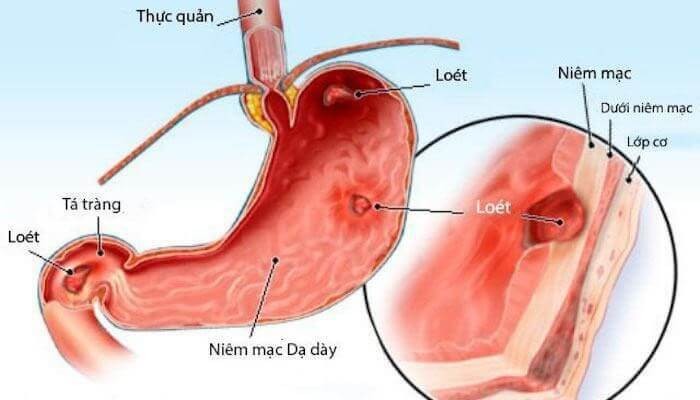
Nuốt phải HClO có thể gây loét dạ dày
6.3. Giao tiếp bằng mắt
HClO có thể gây sưng, đỏ, đau, rách và thậm chí gây mù lòa. Nếu chất này vô tình dính vào mắt bạn hãy nhanh chóng dùng nước sạch rửa sạch liên tục trong 15 phút. Sau đó đến bệnh viện để được hỗ trợ.
6.4. Tiếp xúc với da
Da tiếp xúc với HClO có thể gây phồng rộp, nhiễm trùng, đau và loét. Vì vậy, hãy rửa sạch da bằng nước trong 15 phút. Băng vết thương bằng vải sạch rồi đưa đến bệnh viện cấp cứu.
HClO được biết đến rộng rãi trong nhiều lĩnh vực của đời sống xã hội. Tuy nhiên, cần thận trọng khi tiếp xúc với loại axit này để đảm bảo an toàn cho sức khỏe. Hy vọng những chia sẻ của Trường Chu Văn An đã giúp các bạn hiểu rõ hơn về loại hóa chất này và biết cách ứng dụng vào cuộc sống.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn