Nội dung bài viết
Bảng độ âm điện là yếu tố quan trọng để người ta so sánh tính chất kim loại và phi kim của các nguyên tố hóa học. Nhưng bạn có biết độ âm điện cụ thể đầy đủ của các nguyên tố không?
1. Độ âm điện là gì?
Trước khi xem bảng độ âm điện của các nguyên tố, bạn có biết độ âm điện nghĩa là gì không? Độ âm điện là khả năng của một nguyên tố thu hút các electron xung quanh nó trong liên kết hóa học. Nó sẽ được xác định bởi vị trí của các nguyên tố trong bảng tuần hoàn và sự khác biệt về khả năng hút electron giữa các nguyên tố trong phân tử.
Các nguyên tố có độ âm điện cao sẽ có khả năng hút electron mạnh, đồng thời có xu hướng thu hẹp kích thước liên kết hóa học và tạo ra điện tích âm. Các nguyên tố có độ âm điện thấp có khả năng hút electron yếu hơn và tạo ra điện tích dương.
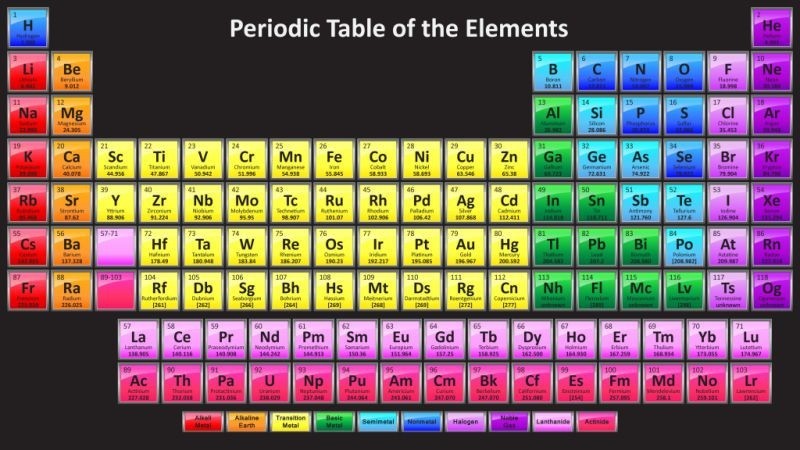
Độ âm điện là gì?
Đây là đại lượng quan trọng để hiểu được tính chất hóa học của phân tử và liên kết hóa học giữa các nguyên tố. Tóm lại:
- Nguyên tử có độ âm điện càng nhỏ thì nguyên tố đó càng có tính kim loại
- Nguyên tử có độ âm điện càng lớn thì tính chất phi kim của nó càng mạnh
- Thang độ âm điện hiện được sử dụng rộng rãi trên toàn thế giới là thang Pauling.
- Độ âm điện nhỏ nhất thường được trao cho Flo vì Flo là kim loại mạnh nhất và sau đó xác định các nguyên tố tiếp theo.
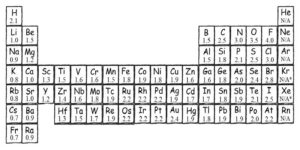
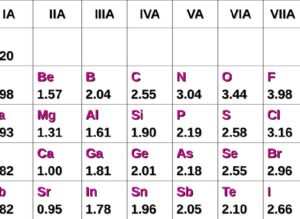
2. Bảng độ âm điện của các nguyên tố hóa học cơ bản
Theo bảng độ âm điện Pauling, nguyên tử Flo sẽ được dùng làm chuẩn để xác định độ âm điện tương đối của các nguyên tử nguyên tố khác. Cụ thể:
Trong một chu kỳ, độ âm điện của các nguyên tử sẽ tăng dần từ trái sang phải theo hướng điện tích hạt nhân.
Trong một nhóm, độ âm điện của các nguyên tử sẽ giảm dần từ trên xuống dưới theo chiều điện tích hạt nhân.
3. Độ âm điện và xu hướng tuần hoàn
Trong một khoảng thời gian đi từ trái sang phải sẽ thấy điện tích hạt nhân có chiều tăng dần. Nhưng kích thước nguyên tử giảm đi. Do đó, giá trị độ âm điện sẽ tăng dần theo thời gian trong bảng tuần hoàn hiện đang được sử dụng.
Số nguyên tử cũng sẽ tăng lên khi bạn di chuyển xuống nhóm của bảng tuần hoàn. Giá trị điện tích hạt nhân cũng tăng lên nhưng một lớp vỏ sẽ được thêm vào để tăng tác dụng của điện tích.
Giá trị độ âm điện cũng sẽ có xu hướng giảm khi bạn di chuyển xuống nhóm nguyên tử. Phi kim sẽ có giá trị độ âm điện cao hơn kim loại. Vì vậy, trong tự nhiên, phi kim có độ âm điện và kim loại có độ âm điện.
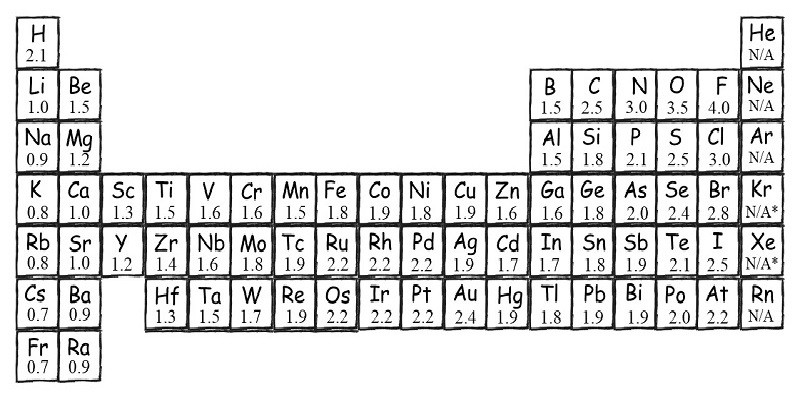
Xu hướng định kỳ của độ âm điện
4. Độ âm điện và các yếu tố ảnh hưởng
Ngoài bảng độ âm điện, chúng ta hãy xem xét các yếu tố ảnh hưởng đến độ âm điện của nguyên tử:
4.1. Kích thước nguyên tử
Đối với các nguyên tử có kích thước lớn, giá trị độ âm điện nhỏ, vì các electron ở xa hạt nhân sẽ chịu ít lực hút từ hạt nhân hơn.
4.2. Điện tích hạt nhân
Hạt nhân có điện tích lớn hơn thì độ âm điện sẽ có giá trị lớn hơn. Đó là bởi vì có sự gia tăng điện tích hạt nhân khiến electron thu hút với lực lớn hơn.
4.3. Tác dụng của chất thay thế
Độ âm điện của một nguyên tử cũng sẽ phụ thuộc vào bản chất của nhóm thế gắn với nguyên tử đó. Chính sự khác biệt về độ âm điện của một nguyên tử do các nhóm thế gây ra sẽ dẫn đến hành vi hóa học khác nhau của nguyên tử đó.
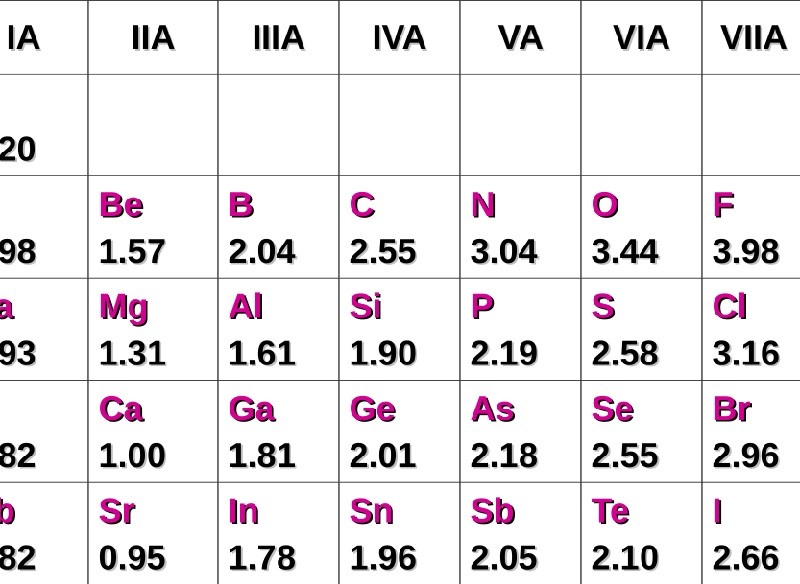
Những yếu tố nào ảnh hưởng đến độ âm điện?
5. Độ âm điện và liên kết hóa học
Hiệu độ âm điện là sự chênh lệch giữa giá trị độ âm điện của nguyên tử của hai nguyên tố hóa học. Dựa vào độ chênh lệch độ âm điện, người ta có thể dự đoán loại liên kết hóa học của phân tử.
Độ chênh lệch độ âm điện cũng có cách tính rất đơn giản. Bạn chỉ cần trừ giá trị lớn hơn của nguyên tử của nguyên tố này khỏi giá trị nhỏ hơn của nguyên tử của nguyên tố kia. Từ độ chênh lệch độ âm điện sẽ có các liên kết hóa học như:
5.1. Liên kết cộng hóa trị không phân cực
Hiệu độ âm điện của các nguyên tử tham gia liên kết hóa học nằm trong khoảng từ 0 đến nhỏ hơn 0,4. Liên kết này được gọi là liên kết cộng hóa trị không phân cực. Độ phân cực của liên kết dưới 0,4, nhỏ đến mức không thể xác định được trong thực tế.
5.2. Liên kết cộng hóa trị có cực
Liên kết cộng hóa trị có cực là liên kết được tạo thành từ các nguyên tử có giá trị độ âm điện nằm trong khoảng từ 0,4 đến dưới 1,7. Giá trị này càng lớn thì độ phân cực sẽ càng cao.
5.3. Liên kết ion
Liên kết ion là liên kết trong đó độ chênh lệch độ âm điện giữa các nguyên tử lớn hơn hoặc bằng 1,7. Các nguyên tử có độ âm điện lớn hơn có khả năng hút các electron đủ mạnh để nhận hoàn toàn các electron từ các nguyên tử còn lại, tạo thành các ion âm. Nguyên tử mất electron trở thành ion dương.
Hy vọng những thông tin về bảng độ âm điện trên sẽ hữu ích giúp bạn có thêm những kiến thức bổ ích.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn