Nội dung bài viết
Quá trình điều chế H2SO4 là gì? Quy trình sản xuất axit sunfuric trong công nghiệp và điều chế h2so4 trong phòng thí nghiệm như thế nào? Tham khảo thông tin trong bài viết sau
Với nhiều ứng dụng hữu ích trong sản xuất, xử lý nước thải và phòng thí nghiệm. Axit sunfuric là một chất không còn xa lạ với chúng ta. Nhưng bạn đã hiểu rõ về quy trình, công nghệ và những tiến bộ trong sản xuất axit sunfuric chưa? Tham khảo thông tin nghiên cứu chi tiết qua bài viết dưới đây cùng Vũ Hoàng nhé!
 Quá trình điều chế H2SO4 là gì?
Quá trình điều chế H2SO4 là gì?
Công nghệ sản xuất axit sunfuric
Công nghệ sản xuất axit sunfuric có 3 công nghệ: công nghệ tiếp xúc, công nghệ NOx và công nghệ CaSO4. Cả ba công nghệ đều có nguyên lý chung là thu giữ SO2 từ các nguyên liệu đầu vào khác nhau. Chẳng hạn như lưu huỳnh, pyrit, chalkopyrit, sphalerit, galena, CaSO4, khí rửa, khí thải có chứa lưu huỳnh oxit,…
Công nghệ sản xuất axit sunfuric hoạt động theo quy luật thu SO2 từ một số vật liệu khác nhau: CaSO4, khí thải có chứa oxit lưu huỳnh, lưu huỳnh,… Sau đó khi sử dụng thiết bị tiếp xúc có sử dụng thêm chất xúc tác, SO2 bị oxy hóa thành SO3. Cuối cùng, qua hấp thụ trong axit loãng, SO3 sẽ trở thành H2SO4. Ngày nay công nghệ sản xuất này bao gồm công nghệ tiếp xúc, công nghệ NOx và công nghệ CaSO4.
Công nghệ tiếp xúc hiện nay là công nghệ sản xuất axit sunfuric hiện đại nhất được sử dụng trên thế giới. Để sản xuất công nghiệp axit sulfuric.
Các giai đoạn sản xuất axit sulfuric
Quá trình sản xuất axit sulfuric trải qua nhiều bước và phản ứng hóa học khác nhau. Tóm tắt toàn bộ quá trình, chúng ta có thể trình bày các giai đoạn sản xuất axit sulfuric như sau:
Bước đầu tiên là điều chế SO2:
Đốt pyrit trong lò dùng để sản xuất khí SO2. Kết quả khi đốt sẽ sinh ra SO2, O2 và một số tạp chất khác. Khi đó hỗn hợp khí SO2 sẽ thu được ở đầu lò. Để loại bỏ tạp chất và O2, chúng tôi tinh chế hỗn hợp thu được để thu được SO2. Tinh chế bằng cách tách tạp chất ra khỏi hỗn hợp bằng các hệ thống chuyên dụng như tách bụi lốc xoáy, tách asen, tách “mù” H2SO4, tách hơi nước,…
Xem thêm: >>> Dung dịch Axit Sunfuric H2SO4
Bước thứ hai sẽ oxy hóa SO2 thành SO3 bằng chất xúc tác rắn (V2O5).
Mức độ chuyển hóa SO2 thành SO3 phụ thuộc vào thời gian tiếp xúc và nhiệt độ. Khi đó, nếu thời gian tiếp xúc của các chất tham gia và chất xúc tác tăng lên thì tốc độ chuyển hóa cũng tăng lên.
Bước cuối cùng là hấp thụ SO3 để tạo thành axit sunfuric. Lúc này SO3 sẽ được xử lý bằng nước bằng cách phản ứng với H2O tạo thành H2SO4.
Một số cải tiến công nghệ sản xuất H2SO4
Với yêu cầu sản xuất ngày càng cao và các yếu tố môi trường. Cần phải cải tiến công nghệ sản xuất H2SO4. Để giải quyết các yêu cầu và vấn đề đó như:
Quy trình điều chế H2SO4 trong phòng thí nghiệm
Quy trình điều chế axit sunfuric (H₂SO₄) trong phòng thí nghiệm bao gồm các bước chính sau:
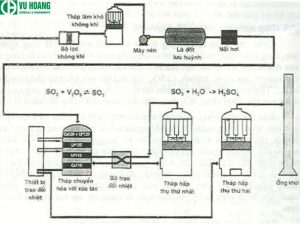 Quy trình sản xuất H2SO4
Quy trình sản xuất H2SO4
Quy trình điều chế H2SO4 1: Đốt lưu huỳnh tạo ra lưu huỳnh dioxit (SO₂)
Phản ứng hóa học:
S+O2→SO2
Lưu huỳnh cháy trong oxy tạo ra khí SO₂ – Đây là phản ứng oxy hóa cơ bản của lưu huỳnh.
Quy trình điều chế H2SO4 2: Oxy hóa SO₂ thành SO₃ bằng chất xúc tác oxit vanadi (V₂O₅)
Phản ứng hóa học:
2SO2+O2→2SO3
Dưới tác dụng của chất xúc tác V₂O₅, SO₂ bị oxy hóa thành SO₃ – Bước quan trọng để tạo ra axit sulfuric.
Quá trình điều chế H2SO4 3: Hấp thụ SO₃ thành axit sunfuric đậm đặc tạo ra ôle (H₂S₂O₇)
Phản ứng hóa học:
SO3+H2SO4→H2S2O7
SO₃ không hòa tan trực tiếp trong nước. Nên hòa tan trong axit sunfuric đậm đặc để tạo ra oleum – một dạng axit sunfuric đậm đặc.
Quy trình điều chế H2SO4 4: Pha loãng oleum thu được axit sunfuric
Phản ứng hóa học:
H2S2O7+H2O→2H2SO4
Oleum được pha loãng với nước để thu được axit sulfuric có nồng độ mong muốn. Quá trình này cần phải được thực hiện cẩn thận để tránh phản ứng tỏa nhiệt mạnh.
Xem thêm: >>> Axit H2SO4 98%, Việt Nam, 35kg/can
Lưu ý khi điều chế axit sunfuric trong phòng thí nghiệm
- Trang bị bảo hộ đầy đủ: Luôn đeo kính an toàn và găng tay chống hóa chất. Quần áo bảo hộ, quần áo chống hóa chất, giày chống trượt và khẩu trang đảm bảo an toàn.
- Tránh tiếp xúc trực tiếp: Axit sulfuric (H₂SO₄) có thể gây bỏng nghiêm trọng nếu tiếp xúc với da, mắt hoặc màng nhầy.
- Sử dụng dụng cụ chuyên dụng: Chỉ sử dụng thùng, chai, thùng phuy hoặc các thiết bị chứa hóa chất chịu axit, tránh sử dụng các vật liệu có tính ăn mòn. Đậy nắp sau khi sử dụng để hạn chế bay hơi.
- Bảo quản đúng cách: Đặt axit sulfuric ở nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp. Và không để gần các chất bazơ hoặc chất khử để tránh phản ứng nguy hiểm.
- Tránh tiếp xúc với chất phản ứng mạnh: H₂SO₄ có thể phản ứng mạnh với bazơ mạnh hoặc chất khử, sinh nhiệt và sinh ra khí độc.
- Nguyên tắc pha loãng: Luôn thêm axit vào nước từ từ và khuấy đều. Tuyệt đối không đổ nước vào axit, vì có thể gây ra phản ứng mãnh liệt và sinh ra lượng nhiệt lớn.
- Kiểm soát khí thải: Sử dụng hệ thống thông gió hoặc thiết bị xả khí để loại bỏ khí độc. Chẳng hạn như SO₂ và SO₃ phát sinh trong quá trình chuẩn bị.
Kết luận
Hy vọng bài viết trên đã mang đến cho các bạn nhiều thông tin tham khảo hữu ích liên quan đến sản xuất axit sunfuric. Nếu bạn cần mua axit. Bạn có thể liên hệ với chúng tôi qua HOTLINE hoặc Website: https://vuhoangco.com.vn để được giải đáp tốt nhất!


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn