Nội dung bài viết
Cồn (hay Alcohol) là một trong những hợp chất hữu cơ quen thuộc nhất, từ cồn sát trùng 70 độ trong tủ thuốc gia đình, dung môi trong sản xuất công nghiệp, cho đến nguyên liệu chính trong đồ uống. Tuy nhiên, đằng sau sự quen thuộc đó là một nhóm hóa chất đa dạng và phức tạp.
Là chuyên gia về hóa chất công nghiệp với hơn 20 năm kinh nghiệm, vietchem nhận thấy có rất nhiều nhầm lẫn phổ biến xung quanh hợp chất này. Bài viết này sẽ phân tích toàn diện AZ của rượu: định nghĩa, phân loại chính xác (rượu bão hòa, rượu đa chức, rượu nguyên sinh) và đặc biệt trả lời dứt khoát câu hỏi học thuật “Rượu có tác dụng với NaOH không?”.
Định nghĩa Rượu là gì?
Về mặt hóa học, Alcohol là hợp chất hữu cơ có chứa nhóm hydroxyl (–OH) liên kết trực tiếp với nguyên tử Carbon NO (nguyên tử carbon chỉ có một liên kết đơn hay còn gọi là lai hóa (sp3).
Công thức chung của rượu mạch hở, đơn chức, bão hòa là CnH2n+1OH (với n>=1).
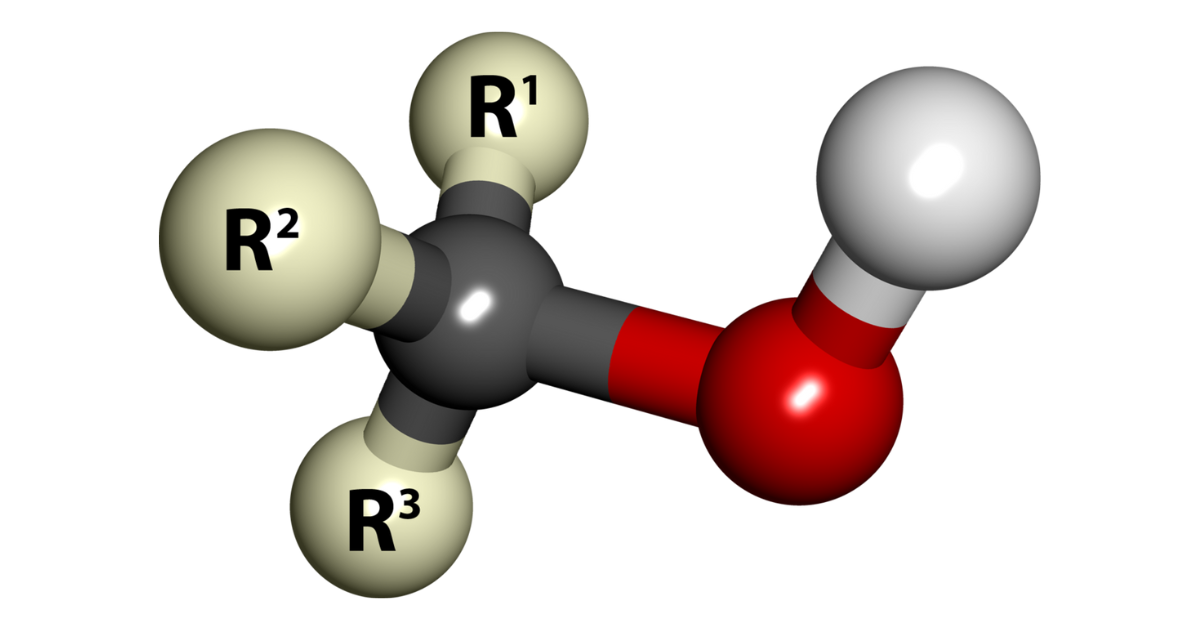
Rượu là gì?
Một số ví dụ phổ biến nhất bao gồm:
- Metanol (CH3OH)
- Etanol (C2H5OH)
Sự khác biệt chính giữa rượu và phenol
Đây là điểm nhầm lẫn lớn nhất trong hóa học hữu cơ, dẫn đến sai sót khi xét phản ứng với NaOH. Mặc dù cả hai đều có nhóm -OH nhưng chúng KHÔNG giống nhau.
Để chứng minh chuyên môn (EAT), vietchem phân biệt rõ ràng giữa 2 nhóm chất này:
|
đặc trưng |
Rượu (Ví dụ: Ethanol, C2H5OH) |
Phenol (Ví dụ: C6H5OH) |
|
Kết cấu |
Nhóm -OH liên kết với Carbon NO (lai hóa sp3). |
Nhóm -OH liên kết trực tiếp với Carbon của vòng benzen (lai hóa sp2). |
|
Hình ảnh |
[Hình ảnh cấu trúc hóa học Ethanol] | [Hình ảnh cấu trúc hóa học Phenol] |
|
Tính axit |
Rất yếu (yếu hơn nước). |
Yếu (nhưng mạnh hơn rượu và nước đáng kể). |
|
Phản ứng với NaOH |
KHÔNG phản ứng. |
CÓ phản ứng CÓ. |
Hiểu được sự khác biệt về cấu trúc này là chìa khóa để trả lời câu hỏi tiếp theo.
Rượu có tác dụng với NaOH không?
Câu trả lời trực tiếp từ ENGCHEM: KHÔNG.
Trong điều kiện phòng thí nghiệm bình thường, Alcohol (ví dụ Ethanol) không phản ứng với các dung dịch bazơ mạnh như Natri Hydroxide (NaOH).
Tại sao Rượu (Ethanol) không phản ứng với NaOH?
Lý do nằm ở tính axit của chúng:
- Tính axit rất yếu: Rượu có tính axit nhưng cực kỳ yếu. Chỉ số pKa (thước đo độ mạnh của một axit, pKa càng lớn thì axit càng yếu) của Ethanol khoảng 16 (Nguồn: PubChem CID 702).
- Yếu hơn nước: Nước (H2O) có pKa khoảng 15,7. Điều này có nghĩa là Ethanol thậm chí còn là một axit yếu hơn cả nước.
- Quy luật phản ứng: Phản ứng axit-bazơ chỉ xảy ra khi axit mạnh tác dụng với bazơ mạnh tạo thành axit yếu hơn và bazơ yếu hơn. Vì Rượu yếu hơn nước nên không thể phản ứng với NaOH để tạo ra H2O (một loại axit mạnh hơn nó).
Tại sao Phenol (C6H5OH) phản ứng với NaOH?
Đây là phần khó hiểu. Không giống như Rượu, Phenol KHÔNG phản ứng với NaOH.
- Nguyên nhân: Do chịu ảnh hưởng của vòng benzen (lực hút electron), liên kết OH của Phenol trở nên phân cực hơn khiến nguyên tử H có tính cơ động cao hơn nhiều so với rượu.
- Chứng minh (pKa): Phenol có pKa chỉ khoảng 9,95 (Nguồn: PubChem CID 996).
- Kết luận: Vì Phenol (pKa 9,95) là một axit mạnh mẽ hơn nước (pKa 15,7) có thể phản ứng hoàn toàn với bazơ mạnh NaOH.
C6H5OH + NaOH -> C6H5ONa (Natri phenolat) + H2O
Đặc tính vật lý và hóa học của rượu
Hiểu rõ những đặc tính này là nền tảng để ứng dụng rượu vào công nghiệp và đời sống.
Tính chất vật lý (Tại sao rượu hòa tan trong nước?)
- Liên kết hydro: Đây là tính chất quan trọng nhất. Các phân tử rượu có thể hình thành liên kết hydro liên phân tử với nhau và với các phân tử nước.
- Hậu quả:
- Điểm sôi: Cao hơn đáng kể so với hydrocarbon hoặc ete có cùng khối lượng phân tử (vì cần nhiều năng lượng hơn để phá vỡ liên kết hydro).
- Độ hòa tan: Các rượu có chuỗi carbon ngắn (như Metanol, Ethanol) hòa tan vô hạn trong nước. Khi chuỗi carbon tăng lên, tính kỵ nước của gốc hydrocarbon tăng lên, làm giảm độ hòa tan.
Tính chất hóa học (Phản ứng điển hình)
Mặc dù không phản ứng với NaOH nhưng rượu vẫn tham gia vào nhiều phản ứng quan trọng:
1. Phản ứng thế H của nhóm -OH (Tính axit yếu):
- Phản ứng với kim loại kiềm mạnh (Na, K) -> giải phóng khí H2.
2C2H5OH + 2Na -> 2C2H5ONa + H2
2. Phản ứng este hóa (với Axit cacboxylic):
- Đây là phản ứng tạo ra este (thơm), cần có chất xúc tác H2SO4 đậm đặc và nhiệt độ.
CH3COOH + C2H5OH <-> CH3COOC2H5 (Ethyl axetat) + H2O
3. Phản ứng khử nước:
- Ở 140°C (xúc tác H2SO4 đậm đặc): Tách nước thành 2 phân tử -> Tạo Ether.
- Ở 170°C (xúc tác H2SO4 đậm đặc): Tách nước nội phân tử -> Tạo Alkene.
4. Phản ứng oxy hóa:
- Đây là phản ứng phụ thuộc chặt chẽ vào nồng độ cồn (sẽ được giải thích ở phần sau).
- Oxy hóa hoàn toàn (Đốt): Luôn tạo ra CO2 và H2O, tỏa nhiều nhiệt.
Phân loại chi tiết Rượu
Để sử dụng đúng và an toàn, vietchem giúp bạn phân loại rượu theo các chỉ tiêu hóa học chính xác.
Phân loại theo cấp độ (Trả lời “Rượu cấp 1 là gì?”)
Bậc của rượu được định nghĩa là bậc của nguyên tử carbon liên kết trực tiếp với nhóm -OH.
- Rượu bậc 1: Nhóm -OH gắn với Carbon sơ cấp (C này chỉ liên kết với 1 C khác).
- Ví dụ: Etanol (CH3-CH2-OH).
- Tính chất oxy hóa: Aldehyd bị oxy hóa nhẹ.
- Rượu bậc hai: Nhóm -OH gắn với Carbon bậc hai (C này liên kết với 2 C khác).
- Ví dụ: Rượu isopropyl (IPA) (CH3-CH(OH)-CH3).
- Tính chất oxy hóa: Bị oxy hóa nhẹ -> Xeton. [Hình ảnh cấu trúc alcohol bậc 2]
- Rượu bậc ba: Nhóm -OH gắn với Carbon bậc ba (C này liên kết với 3 C khác).
- Ví dụ: tert-Butanol.
- Tính chất oxy hóa: Rất khó bị oxy hóa trong điều kiện bình thường (liên kết CC mạnh).
Phân loại theo nguồn gốc hydrocarbon (Trả lời “Không có rượu là gì?”)
- Alcohol No (Alcohol No): Đây là loại phổ biến nhất. Gốc hydrocarbon liên kết với nhóm -OH là gốc bão hòa (chỉ chứa một liên kết đơn).
- Ví dụ: Metanol, Ethanol, Propanol.
- Rượu không bão hòa: Một bazơ hydrocarbon có chứa liên kết đôi hoặc ba.
- Ví dụ: Rượu allylic (CH2=CH-CH2-OH).
- Rượu thơm: Nhóm -OH không phải gắn trực tiếp vào vòng benzen nhưng gắn vào nhánh cacbon bão hòa.
- Ví dụ: Rượu benzylic (C6H5-CH2-OH). (Lưu ý: Chất này vẫn là rượu chứ không phải phenol).
Phân loại theo số nhóm -OH (Trả lời “Rượu đa chức năng”)
- Rượu đơn chức: Phân tử chỉ chứa một nhóm -OH.
- Ví dụ: Hầu hết các ví dụ trên (Ethanol, Metanol, IPA).
- Rượu Đa Chức Năng (Polyol/Polyalcohol): Phân tử chứa hai hoặc nhiều nhóm -OH.
- Tính năng ( ENGCHEM Insight): Vì chúng có nhiều nhóm -OH nên tạo thành nhiều liên kết hydro nên có nhiệt độ sôi rất cao, độ nhớt lớn và khả năng dưỡng ẩm tuyệt vời.
- Ví dụ phổ biến:
- Ethylene Glycol (C2H4(OH)2): Được sử dụng trong sản xuất chất chống đông và nhựa PET.
- Glycerol (Glycerin) (C3H5(OH)3): Được sử dụng trong mỹ phẩm, dược phẩm và thực phẩm. [Hình ảnh cấu trúc hóa học Glycerol
Ứng dụng thực tiễn của các loại Alcohol phổ biến trong công nghiệp
Với tư cách là nhà cung cấp hóa chất công nghiệp, Trường Chu Văn An hiểu rõ giá trị của từng loại alcohol:
1. Methanol (CH3OH):
- Dung môi công nghiệp: Dùng trong sản xuất sơn, mực in, làm chất tẩy rửa.
- Nguyên liệu: Sản xuất formaldehyde, acid acetic.
- Nhiên liệu: Dùng làm nhiên liệu thay thế.
2. Ethanol (C2H5OH):
- Y tế & Sát khuẩn: Thành phần chính của cồn 70°, 90° (cồn y tế) để khử trùng.
- Nhiên liệu: Xăng sinh học (E5, E10) là hỗn hợp của xăng và ethanol.
- Thực phẩm: Thành phần chính của đồ uống có cồn (bia, rượu).
- Dung môi: Dùng trong nước hoa, mỹ phẩm.
3. Isopropyl Alcohol (IPA) (C3H7OH):
- Dung môi (Thế mạnh Trường Chu Văn An): Là dung môi tẩy rửa tuyệt vời cho linh kiện điện tử, vi mạch, đầu từ… vì bay hơi nhanh và không để lại cặn.
- Sát khuẩn: Dùng trong dung dịch sát khuẩn tay và vệ sinh bề mặt.
4. Glycerol (C3H5(OH)3
- Mỹ phẩm & Dược phẩm: Là chất giữ ẩm (humectant) hàng đầu, có mặt trong kem dưỡng da, kem đánh răng.
- Thực phẩm: Chất tạo ngọt, giữ ẩm trong thực phẩm.

Ứng dụng thực tiễn của các loại Alcohol phổ biến trong công nghiệp
Cảnh báo An toàn (SDS) và Rủi ro khi sử dụng Alcohol
CẢNH BÁO TỬ VONG: Tuyệt đối không nhầm lẫn Methanol và Ethanol
- Ethanol (Cồn thực phẩm/y tế): Có thể uống (trong giới hạn) hoặc dùng sát khuẩn.
- Methanol (Cồn công nghiệp): LÀ CHẤT CỰC ĐỘC.
- Chỉ cần uống một lượng rất nhỏ Methanol (vài ml) cũng có thể gây mù lòa vĩnh viễn do phá hủy dây thần kinh thị giác.
- Uống lượng lớn hơn (10-30ml) có thể dẫn đến tử vong.
- Luôn kiểm tra nguồn gốc, nhãn mác. Tuyệt đối không uống cồn không rõ nguồn gốc hoặc cồn công nghiệp.
An toàn Cháy nổ (GHS/SDS)
- Hầu hết các alcohol (Methanol, Ethanol, IPA) đều là chất lỏng rất dễ cháy (Loại 2 hoặc 3 theo Hệ thống hài hòa toàn cầu GHS).
- Hơi của chúng nặng hơn không khí và có thể lan xa đến nguồn lửa gây bắt cháy hoặc nổ.
- Biện pháp PCCC: Luôn lưu trữ trong thùng chứa kín, nơi thoáng mát, tránh xa tuyệt đối mọi nguồn nhiệt, tia lửa điện, ngọn lửa trần. [Hình ảnh biểu tượng GHS dễ cháy]
Lưu trữ và sử dụng an toàn
- Luôn đeo đồ bảo hộ (găng tay, kính) khi tiếp xúc với cồn công nghiệp nồng độ cao.
- Làm việc ở nơi thông thoáng để tránh hít phải hơi.
- Tham khảo kỹ Bảng dữ liệu an toàn hóa chất (SDS – Safety Data Sheet) do nhà cung cấp (chẳng hạn như Trường Chu Văn An) cung cấp trước khi sử dụng.
Mua hóa chất cồn công nghiệp (IPA, Metanol, Glycerol) ở đâu uy tín?
Lựa chọn nhà cung cấp hóa chất uy tín là yếu tố then chốt để đảm bảo an toàn sản xuất và chất lượng thành phẩm.
Với hơn 20 năm kinh nghiệm trong ngành, vietchem tự hào là nhà phân phối hóa chất công nghiệp hàng đầu tại Việt Nam. Chúng tôi cam kết:
- Chất lượng đảm bảo: Cung cấp đầy đủ các loại Cồn công nghiệp (Manol, IPA, Ethanol công nghiệp, Glycerol…) với chất lượng nguyên chất, ổn định.
- Nguồn gốc rõ ràng: Sản phẩm có đầy đủ giấy tờ, Giấy chứng nhận phân tích (COA) và Bảng dữ liệu an toàn hóa chất (SDS).
- An toàn và chuyên nghiệp: Hệ thống kho bãi hiện đại, tuân thủ nghiêm ngặt công tác phòng cháy chữa cháy. Đội ngũ kỹ thuật viên của chúng tôi sẵn sàng tư vấn giải pháp và an toàn khi sử dụng.
Nếu bạn đang tìm kiếm nguồn cung cấp Metanol, Isopropyl Alcohol (IPA), Glycerol hay các dung môi công nghiệp khác hãy liên hệ ngay với Trường Chu Văn An để nhận được tư vấn kỹ thuật và báo giá tốt nhất.



Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn