Nội dung bài viết
Axit sunfuric 98% (H2SO4): Cách điều chế và ứng dụng trong đời sống. Axit sunfuric (H2SO4) nổi tiếng là “Vua hóa chất”. Bởi chúng là những hóa chất có vai trò và ứng dụng cao trong cuộc sống ngày nay. Để giúp các bạn hiểu rõ hơn về tính chất hóa học, cách điều chế và ứng dụng thực tế của axit sunfuric. Vậy thì hãy cùng Vũ Hoàng tham khảo ngay bài viết chia sẻ dưới đây nhé.
 Axit Sunfuric 98% (H2SO4): Cách điều chế và ứng dụng trong đời sống
Axit Sunfuric 98% (H2SO4): Cách điều chế và ứng dụng trong đời sống
Tìm hiểu tổng quan về Axit Sunfuric 98% (H2SO4)
Trước khi chúng ta tìm hiểu thêm về cách điều chế axit sulfuric hoặc các ứng dụng của nó. Sau đây là một số thông tin cơ bản về loại axit này cũng như các tính chất vật lý và hóa học của axit sulfuric:
Axit sunfuric 98% (H2SO4) là gì?
H2SO4 là công thức hóa học của Axit Sunfuric (axit sunfuric). Một axit vô cơ được tạo thành từ các nguyên tố như (S) – Lưu huỳnh, (O) – Oxy và (H) – Hydro. Axit này được biết đến với nhiều tên gọi khác nhau như axit sunfuric, dầu sunfat, hydro sunfat.
Tính chất vật lý của axit sunfuric 98% (H2SO4)
Axit sunfuric là chất lỏng nhớt giống như dầu. Nó là một axit không màu, không mùi, hòa tan vô hạn trong nước. Có thể hòa tan trong hầu hết các dung môi hữu cơ. Chúng rất khát nước nên khi kết hợp với H2O có thể tạo ra lượng nhiệt rất cao. Đặc biệt, axit H2SO4 còn có khả năng cacbon hóa các hợp chất hữu cơ
Nhiệt độ sôi của axit sunfuric là 336 độ C, nhiệt độ nóng chảy là 10,371 độ C.
Tính chất hóa học của axit sunfuric 98% (H2SO4)
Trong số các hóa chất, axit sunfuric có tính axit rất mạnh. Có thể ăn mòn nhiều đồ vật khác và gây nguy hiểm cho bất cứ thứ gì chúng tiếp xúc nếu nồng độ axit vượt quá mức cho phép. Vì vậy, một số công đoạn điều chế và phản ứng hóa học với axit này sẽ cần phải có sự chuẩn bị cẩn thận. Nếu không sẽ rất dễ xảy ra hỏa hoạn, gây bỏng nặng, bắn vào mắt có thể gây mù lòa…
Axit này cũng đóng một vai trò rất quan trọng trong việc điều chế các axit dễ bay hơi. Từ các muối axit khác vì chúng có độ bay hơi khá thấp. Nhờ tính chất ưa nước, axit sulfuric còn có thể được sử dụng để làm khô các khí không phản ứng với axit. Trong một số phản ứng hóa học H2SO4 không phản ứng ở nhiệt độ thường. Nhưng có thể nếu thêm nhiều nhiệt hơn như phản ứng với (Al) – nhôm, (Fe) – sắt.
Axit sulfuric có thể được xác định thông qua quỳ tím (quỳ tím chuyển sang màu đỏ khi cho axit vào). Trong hóa học, H2SO4 tồn tại ở hai dạng: rắn và loãng.
Xem thêm: >>> Dung dịch axit sunfuric H2SO4
Tính chất phân cực và độ dẫn điện của axit sulfuric
Axit sulfuric tinh khiết là chất phân cực, có hệ số điện môi xấp xỉ 100. Các phân tử H2SO4 có thể proton hóa lẫn nhau, tạo thành điện cực dẫn điện. Quá trình này còn được gọi là di chuyển proton.
Cách điều chế axit sunfuric
Việc điều chế H2SO4 có thể được thực hiện bằng nhiều phương pháp khác nhau tùy theo quy mô sản xuất. Sau đây là hai phương pháp chính: chuẩn bị công nghiệp và phòng thí nghiệm
Điều chế axit sunfuric 98% (H2SO4) trong công nghiệp
Để điều chế axit sunfuric, bạn có thể thực hiện theo quy trình sau: sử dụng S hoặc FeS2 -> SO2 -> SO3 -> H2SO4
- Đốt quặng pyrit sắt thu được SO2: 4FeS2 + 11O2 -> 8SO2 + 2Fe2O3
- Oxy hóa SO2 bằng oxy ở nhiệt độ từ 400 độ C – 5000 độ C, sử dụng xúc tác V2O5 (Vanadium Pentoxide): 2SO2 + O2 -> 8SO3
- Dùng H2SO4 đậm đặc hấp thụ SO3 tạo ra ôle có công thức H2SO4.nSO3: nSO3 + H2SO4 -> H2SO4.nSO3
- Pha loãng ôle thành H2SO4 với lượng nước thích hợp: H2SO4.nSO3 + (n+1) H2O -> (n+1)H2SO4
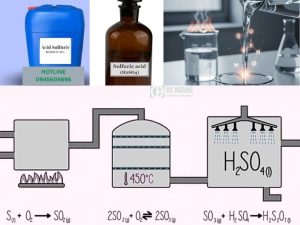 Phương pháp điều chế H2SO4
Phương pháp điều chế H2SO4
Điều chế axit sunfuric 98% (H2SO4) trong phòng thí nghiệm
Việc điều chế H2SO4 trong phòng thí nghiệm chưa thực sự phổ biến. Do các thiết bị đặc biệt và các mối nguy hiểm và yêu cầu về an toàn. Tuy nhiên, một số phản ứng sau đây có thể được thực hiện:
Phương pháp chuẩn bị đơn giản
Một phương pháp phổ biến trong phòng thí nghiệm là tạo ra SO₃. Từ phản ứng giữa natri bisulfat và kali dicromat rồi hòa tan SO₃ trong nước.
- Tạo SO₃: NaHSO4 + K2Cr2O7 + H2SO4 → K2SO4 + Na2SO4 + Cr2(SO4)3 + H2O (Trong phản ứng này, SO₃ được tạo ra)
- Hòa tan SO₃ trong nước: SO3+H2O→H2SO4
Phương pháp điện phân
Phương pháp này liên quan đến việc điện phân dung dịch CuSO₄ (đồng sunfat) trong nước.
- Điện phân CuSO₄: 2H2O → O2 + 4H+ + 4e− (Ở cực dương, nước phân hủy thành ion oxy và hydro)CuSO4 → Cu2+ + SO42− (Ở cực âm, đồng bị ion hóa và ion sunfat)
- Kết hợp H⁺ và SO₄²⁻: 4H+ + SO42− → H2SO4
Xem thêm: >>> Axit sulfuric là gì? Đặc điểm, ứng dụng và những lưu ý khi sử dụng H2SO4
Ứng dụng của H2SO4 rất phổ biến trong đời sống
Tuy là một loại axit nhưng có rất nhiều điều cần lưu ý và chú ý trong quá trình sử dụng. Nhưng bên cạnh đó, axit H2SO4 còn mang đến vô số ứng dụng hữu ích cho đời sống con người ngày nay. Những ứng dụng phổ biến của axit sunfuric trong đời sống ngày nay bao gồm:
Trong công nghiệp
Axit sunfuric được sử dụng để sản xuất nhiều loại kim loại (kẽm, đồng, v.v.). Và chúng còn là thành phần trong các dung dịch dùng để tẩy vết rỉ sét, làm sạch bề mặt kim loại… Chúng còn được dùng để sản xuất nhôm sunfat, làm chất nổ, thuốc nhuộm, thuốc nhuộm, giấy, dược phẩm, v.v.
Dùng để xử lý chất thải
H2SO4 còn được dùng để sản xuất AlOH3 – nhôm hydroxit. Đây là chất dùng để lọc các tạp chất có trong nước thải. Giúp trung hòa độ pH trong nước, loại bỏ nước cứng (nước có ion Ca2+, Mg+) và giúp cải thiện mùi vị của nước.
Bộ lọc dầu
Axit sulfuric thường được kết hợp với một axit khác. Để giúp loại bỏ các hợp chất lưu huỳnh hoặc hydrocacbon không bão hòa trong dầu thô. Đây được biết đến là phương pháp lọc dầu khá phổ biến.
Sản xuất phân bón
Sử dụng H2SO4 để tạo ra axit photphoric – chất dùng để sản xuất phân bón như amoni sunfat, photphat,…
Áp dụng vào y học và điều trị
Những ứng dụng của axit sulfuric trong lĩnh vực y học và điều trị cũng vô cùng nổi bật. Chẳng hạn như tạo ra hóa trị liệu alkyl hóa để ngăn ngừa và chống lại bệnh ung thư ở người.
Sản xuất pin
Một ứng dụng cực kỳ phổ biến của axit sulfuric là ở dạng pha loãng. Nó được sử dụng làm chất điện phân để liên kết các bộ phận của pin lại với nhau để tạo ra pin axit. Ắc quy axit được sử dụng để các thiết bị điện, động cơ, máy móc hoạt động và vận hành.
Kết luận
Trên đây là bài viết chia sẻ liên quan đến việc điều chế và ứng dụng axit sunfuric trong đời sống ngày nay. Cùng với đó là địa chỉ uy tín mà bạn có thể tin tưởng để lựa chọn mua hóa chất chất lượng cho mình.
Vũ Hoàng hiện là đơn vị hàng đầu chuyên phân phối hóa chất nhập khẩu. Với chất lượng cao đến tay người dùng Việt Nam với mức giá cực kỳ hợp lý.
Vui lòng liên hệ với chúng tôi qua HOTLINE hoặc Website: https://vuhoangco.com.vn để được báo giá chi tiết.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn