Nội dung bài viết
Giới thiệu
Axit clohydric (HCl) là một hợp chất vô cơ mạnh có nhiều ứng dụng trong công nghiệp và phòng thí nghiệm. Trong công nghiệp, axit clohydric 35% được sản xuất bằng cách đốt khí hydro và khí clo ở nhiệt độ cao. Quá trình này đòi hỏi phải cẩn thận vì axit clohydric có tính ăn mòn mạnh và có thể gây cháy nếu tiếp xúc với một số chất.
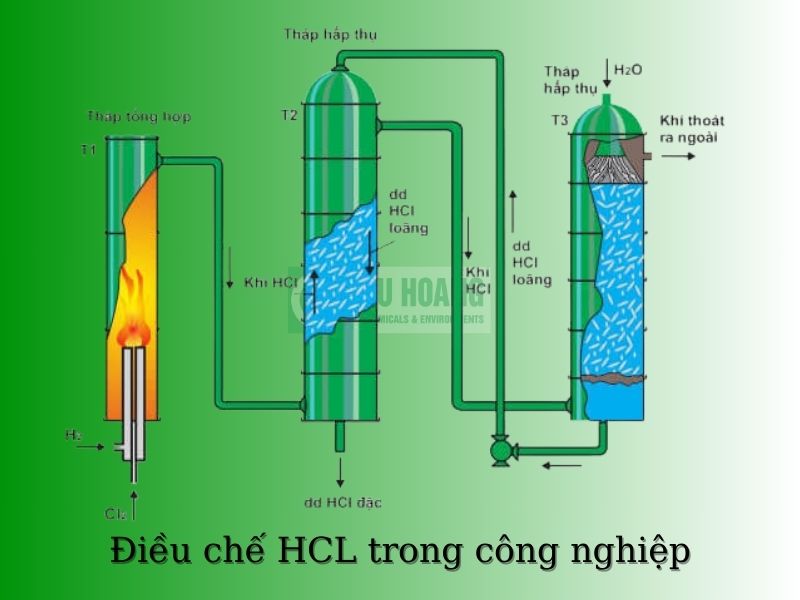
Phương pháp đốt khí hydro và khí clo
Phương pháp đốt khí hydro và clo là phương pháp phổ biến nhất để sản xuất axit clohydric 35% trong công nghiệp. Quá trình này bắt đầu bằng việc sản xuất khí hydro và khí clo thông qua quá trình điện phân dung dịch muối (NaCl) bằng màng. Sau đó, cả hai loại khí này sẽ được đưa vào bình đốt ở nhiệt độ cao sẽ thu được khí HCl. Phản ứng hóa học trong quá trình này là:
H2 + Cl2 → 2HCl
Điều kiện phản ứng
- Nhiệt độ: 400°C
- Áp suất: 10 atm
- Tỷ lệ mol ##Cl2 = 1:1
Lợi thế
- Sản lượng cao
- Hiệu suất phản hồi tốt
- Chi phí sản xuất thấp
Nhược điểm
- Cần sử dụng khí clo độc, dễ cháy
- Phản ứng toả nhiều nhiệt nên cần làm nguội bình phản ứng
- Axit clohydric thu được có thể bị nhiễm tạp chất
Quy trình sản xuất
- Bước 1: Sản xuất khí hydro và khí clo
Khí hydro và khí clo được tạo ra bằng cách điện phân dung dịch muối (NaCl) qua màng. Quá trình điện phân được thực hiện trong bể điện phân chứa dung dịch NaCl bão hòa. Khi dòng điện chạy qua dung dịch, các ion Na+ và Cl- sẽ bị tách thành các nguyên tử riêng biệt. Các nguyên tử hydro sẽ di chuyển về cực âm, tạo thành khí hydro, còn nguyên tử clo sẽ di chuyển về cực dương, tạo thành khí clo.
- Bước 2: Đốt cháy khí hydro và khí clo
Khí hydro và clo được đưa vào thùng đốt ở nhiệt độ cao và áp suất cao. Khi hai khí này tiếp xúc với nhau sẽ phản ứng với nhau tạo thành khí HCl. Phản ứng này tỏa rất nhiều nhiệt nên đầu đốt phải được làm mát bằng nước hoặc không khí.
- Bước 3: Làm nguội và hấp thụ khí HCl
Khí HCl thu được từ quá trình đốt cháy được làm mát bằng cách cho nó đi qua bình làm mát. Khí HCl sau đó được hấp thụ vào nước tạo thành dung dịch axit clohydric. Nồng độ của dung dịch axit clohiđric phụ thuộc vào lượng nước dùng để hấp thụ khí HCl.
- Bước 4: Tinh chế axit clohydric
Dung dịch axit clohydric thu được từ quá trình hấp thụ có thể bị nhiễm tạp chất, chẳng hạn như khí clo dư, khí hydro dư và muối kim loại. Để tinh chế axit clohydric, người ta có thể sử dụng các phương pháp như chưng cất phân đoạn, khử ion hoặc thẩm thấu ngược.
Axit clohydric 35% được sử dụng rộng rãi trong công nghiệp, có tính axit và oxi hóa khử mạnh. Nó được áp dụng trong:
- Làm sạch: Axit clohydric được sử dụng để làm sạch bề mặt kim loại, loại bỏ rỉ sét và các chất bẩn khác.
- Sản xuất các chất hữu cơ và vô cơ: Axit clohydric được sử dụng để sản xuất nhiều loại hợp chất hữu cơ và vô cơ, như thuốc nhuộm, thuốc trừ sâu, phân bón và các hóa chất khác.
- Trung hòa pH: Axit clohydric được sử dụng để trung hòa độ pH của nước thải và các chất lỏng khác.
- Là chất trung gian hóa học: Axit clohydric được sử dụng làm chất trung gian hóa học để tạo ra các sản phẩm hóa học khác, như clorua sắt, clorua nhôm và clorua kẽm.
Những lưu ý khi sử dụng axit clohydric 35%
Axit clohydric 35% là chất ăn mòn mạnh và có thể gây cháy nếu tiếp xúc với một số chất. Vì vậy, khi sử dụng axit clohydric cần tuân thủ các biện pháp an toàn sau:
- Tránh tiếp xúc trực tiếp với axit clohydric.
- Sử dụng quần áo bảo hộ, găng tay và kính bảo hộ khi làm việc với axit clohydric.
- Không để axit clohydric tiếp xúc với các chất dễ cháy, nổ hoặc có tính oxy hóa mạnh.
- Bảo quản axit clohydric trong hộp chuyên dụng có nắp đậy kín và để xa tầm tay trẻ em.
Cách điều chế axit clohydric trong phòng thí nghiệm
Trong phòng thí nghiệm, axit clohydric cũng có thể được điều chế thông qua các phản ứng sau:
- Phản ứng giữa NaCl (rắn) và H2SO4 (đậm đặc):
NaCl + H2SO4 → NaHSO4 + HCl
- Phản ứng giữa kim loại kiềm và axit clohiđric:
Na + HCl → NaCl + H2
Những điều cần biết về axit clohiđric 35%
- Axit clohydric 35% là dung dịch trong suốt, không màu, có mùi hăng.
- Axit clohydric 35% có tính ăn mòn mạnh và có thể gây bỏng da nếu tiếp xúc trực tiếp.
- Axit clohydric 35% có thể phản ứng với một số kim loại như nhôm, sắt và kẽm để tạo thành khí hydro.
- Axit clohydric 35% là chất độc hại và có thể gây tử vong nếu nuốt phải.
- Axit clohydric 35% được sử dụng rộng rãi trong công nghiệp và phòng thí nghiệm.
Câu hỏi thường gặp
- Axit clohydric 35% được sản xuất như thế nào?
Axit clohydric 35% được tạo ra bằng cách đốt khí hydro và khí clo ở nhiệt độ cao.
- Công dụng của axit clohydric 35% là gì?
Axit clohydric 35% được sử dụng rộng rãi trong công nghiệp, có tính axit và oxi hóa khử mạnh. Nó được ứng dụng trong làm sạch, sản xuất hữu cơ và vô cơ, trung hòa độ pH và làm chất trung gian hóa học để tạo ra các sản phẩm hóa học khác.
- Axit clohydric 35% có nguy hiểm không?
Axit clohydric 35% là chất ăn mòn mạnh và có thể gây cháy nếu tiếp xúc với một số chất. Vì vậy, khi sử dụng axit clohydric phải tuân thủ các biện pháp an toàn.
- Làm thế nào để sử dụng axit clohydric 35% một cách an toàn?
Khi sử dụng axit clohydric 35% phải tuân thủ các biện pháp an toàn sau:
- Tránh tiếp xúc trực tiếp với axit clohydric.
- Sử dụng quần áo bảo hộ, găng tay và kính bảo hộ khi làm việc với axit clohydric.
- Không để axit clohydric tiếp xúc với các chất dễ cháy, nổ hoặc có tính oxy hóa mạnh.
- Bảo quản axit clohydric trong hộp chuyên dụng có nắp đậy kín và để xa tầm tay trẻ em.
- Axit clohydric 35% có thể được điều chế trong phòng thí nghiệm?
Trong phòng thí nghiệm, axit clohydric cũng có thể được điều chế thông qua phản ứng giữa NaCl (rắn) và H2SO4 (đậm đặc), hoặc phản ứng giữa kim loại kiềm và axit clohydric.

Kết luận
Axit clohydric 35% là một hợp chất vô cơ mạnh có nhiều ứng dụng trong công nghiệp và phòng thí nghiệm. Phương pháp phổ biến nhất để sản xuất công nghiệp axit clohydric 35% là đốt khí hydro và khí clo ở nhiệt độ cao. Axit clohydric 35% có tính ăn mòn mạnh và có thể gây cháy nếu tiếp xúc với một số chất, vì vậy phải tuân thủ các biện pháp an toàn khi sử dụng.
Tóm tắt các điểm chính:
- Axit clohydric 35% được tạo ra bằng cách đốt khí hydro và khí clo ở nhiệt độ cao.
- Axit clohydric 35% có tính ăn mòn mạnh và có thể gây cháy nếu tiếp xúc với một số chất.
- Axit clohydric 35% được sử dụng rộng rãi trong công nghiệp, có tính axit và oxi hóa khử mạnh.
- Khi sử dụng axit clohydric 35% phải tuân thủ các biện pháp an toàn.
- Trong phòng thí nghiệm, axit clohydric cũng có thể được điều chế thông qua phản ứng giữa NaCl (rắn) và H2SO4 (đậm đặc), hoặc phản ứng giữa kim loại kiềm và axit clohydric.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn