Nội dung bài viết
Cách tạo HCl – Phương pháp điều chế và ứng dụng công nghiệp. Axit clohydric (HCl) là một trong những hợp chất hóa học quan trọng trong nhiều lĩnh vực công nghiệp và nghiên cứu khoa học. Nó không chỉ có tính ăn mòn mạnh. Nó cũng là thành phần thiết yếu trong quá trình sản xuất nhiều loại hóa chất khác nhau. Hiểu cách tạo ra HCl không chỉ giúp ích cho các nhà hóa học. Nhưng nó cũng cung cấp cái nhìn sâu sắc cho những người làm việc trong môi trường công nghiệp. Trường hợp việc sử dụng HCl thường xuyên được áp dụng. Trong bài viết này hãy cùng Hóa chất Vũ Hoàng tìm hiểu chi tiết cách tạo ra HCl. Từ những phản ứng hóa học cơ bản nhất đến quy trình sản xuất công nghiệp.
 Cách tạo HCl – Phương pháp điều chế và ứng dụng công nghiệp
Cách tạo HCl – Phương pháp điều chế và ứng dụng công nghiệp
Tính chất lý hóa của HCl (Axit clohiđric)
Axit clohydric (HCl) là một hợp chất hóa học quan trọng. Có nhiều ứng dụng trong công nghiệp và phòng thí nghiệm. HCl tồn tại ở cả dạng khí (hydro clorua) và dạng dung dịch (axit clohydric).
Tính chất vật lý:
- Trạng thái: Ở điều kiện thường, HCl là chất khí không màu, có mùi mạnh và nặng hơn không khí. Khi tan trong nước, HCl tạo thành dung dịch không màu, có vị chua.
- Độ hòa tan: HCl hòa tan rất tốt trong nước. Dung dịch HCl đậm đặc có nồng độ tối đa khoảng 37% khối lượng.
- Tính dẫn điện: Dung dịch HCl dẫn điện tốt do có khả năng phân ly hoàn toàn thành các ion H+ và Cl-.
- Độ bay hơi: HCl dễ bay hơi, đặc biệt khi đun nóng dung dịch HCl đậm đặc.
Tính chất hóa học:
- Tính axit mạnh: HCl là một trong những axit mạnh nhất, làm quỳ tím chuyển sang màu đỏ.
- Phản ứng với kim loại: Phản ứng với nhiều kim loại (trừ Cu, Ag, Au, Pt,…) tạo thành muối clorua và khí hydro.
- Ví dụ: Fe + 2HCl → FeCl₂ + H₂
- Phản ứng với bazơ: Tác dụng với bazơ tạo thành muối và nước.
- Ví dụ: HCl + NaOH → NaCl + H₂O
- Phản ứng với oxit bazơ: Phản ứng với oxit bazơ tạo thành muối và nước.
- Ví dụ: HCl + CaO → CaCl₂ + H₂O
- Phản ứng với muối: Phản ứng với một số muối tạo thành muối mới và axit mới (điều kiện: sản phẩm phải có kết tủa hoặc khí thoát ra).
- Ví dụ: 2HCl + Na₂CO₃ → 2NaCl + CO₂↑ + H₂O
- Phản ứng với kim loại: Phản ứng với nhiều kim loại (trừ Cu, Ag, Au, Pt,…) tạo thành muối clorua và khí hydro.
- Tính khử: Trong một số trường hợp, HCl thể hiện tính khử khi phản ứng với các chất oxy hóa mạnh như KMnO₄, MnO₂, KClO₃,…
Xem thêm: >>> Tác dụng của HCl trong đời sống và sản xuất công nghiệp
Cách tạo HCl trong công nghiệp
HCl (axit clohydric) là một hóa chất quan trọng được sử dụng rộng rãi trong nhiều ngành công nghiệp. Dưới đây là các phương pháp chính để sản xuất HCl quy mô lớn:
Cách tạo ra HCl từ phản ứng giữa clo và hydro:
- Nguyên tắc: Đây là phương pháp tổng hợp trực tiếp, hiệu quả và được sử dụng phổ biến nhất. Khí hydro (H₂) và khí clo (Cl₂) khi đốt ở nhiệt độ cao tạo thành HCl.
- Phương trình phản ứng: H₂ + Cl₂ → 2HCl
- Lợi thế:
- Sản phẩm thu được có độ tinh khiết cao.
- Năng suất lớn.
- Quá trình sản xuất diễn ra liên tục và dễ kiểm soát.
Cách tạo HCl từ muối natri và axit sunfuric:
- Nguyên tắc: Muối natri clorua (NaCl) phản ứng với axit sunfuric đậm đặc tạo thành natri sunfat và khí HCl.
- Phương trình phản ứng:
- NaCl + H₂SO₄ → NaHSO₄ + HCl (ở nhiệt độ thấp)
- 2NaCl + H₂SO₄ → Na₂SO₄ + 2HCl (ở nhiệt độ cao)
- Ưu điểm: Nguyên liệu dễ tìm và rẻ.
- Nhược điểm: Sản phẩm thu được có thể chứa tạp chất. Và hiệu suất phản ứng không cao bằng phương pháp tổng hợp trực tiếp.
Được sản xuất thông qua quy trình chloralkali:
- Nguyên tắc: Điện phân dung dịch muối ăn bão hòa (NaCl) có màng. Để sản xuất clo, natri hydroxit (NaOH) và khí hydro. Khí hydro thu được có thể kết hợp lại với clo để tạo thành HCl.
- Phương trình phản ứng: (như đã trình bày ở câu hỏi trước)
- Ưu điểm: Sản xuất cùng lúc nhiều sản phẩm có giá trị.
- Nhược điểm: Yêu cầu thiết bị điện phân phức tạp và tiêu tốn nhiều năng lượng.
Sản xuất HCl từ quá trình clo hóa các hợp chất hữu cơ:
- Nguyên tắc: Trong quá trình sản xuất các hợp chất hữu cơ. Giống như vinyl clorua (được sử dụng để sản xuất PVC), một lượng lớn HCl được tạo ra dưới dạng sản phẩm phụ.
- Ưu điểm: Tận dụng được nguồn nguyên liệu sẵn có.
- Nhược điểm: Độ tinh khiết của HCl thu được có thể không cao và phụ thuộc vào quá trình sản xuất sơ cấp.
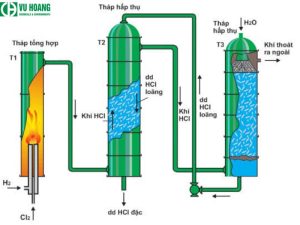 Sơ đồ thiết bị sản xuất axit clohydric (HCl) công nghiệp
Sơ đồ thiết bị sản xuất axit clohydric (HCl) công nghiệp
Xem thêm: >>> Axit Clohydric – Axit HCl 32% – Axit Clohydric
Cách điều chế HCl trong phòng thí nghiệm
Trong phòng thí nghiệm, HCl thường được điều chế ở quy mô nhỏ để sử dụng trong các thí nghiệm. Dưới đây là hai phương pháp phổ biến:
Dùng axit sunfuric để tạo HCl:
- Nguyên tắc: Muối clorua (thường là NaCl) phản ứng với axit sunfuric đậm đặc tạo ra khí HCl.
- Phương trình phản ứng:
- NaCl(r) + H₂SO₄(đậm đặc) → NaHSO₄ + HCl↑ (
- 2NaCl(r) + H₂SO₄(đậm đặc) → Na₂SO₄ + 2HCl↑ (> 400°C)
- Ưu điểm: Cách làm đơn giản, nguyên liệu dễ tìm.
- Nhược điểm: Khí HCl thu được có thể chứa tạp chất. Và hiệu suất phản ứng không cao bằng phương pháp công nghiệp.
Cách tạo HCl từ quá trình thủy phân các hợp chất chứa clorua:
- Nguyên tắc: Một số hợp chất có chứa clorua khi phản ứng với nước sẽ tạo ra HCl.
- Ví dụ: Phosphoryl clorua (POCl₃): POCl₃ + 3H₂O → H₃PO₄ + 3HCl
- Ưu điểm: Phương pháp này có thể sử dụng cho các hợp chất chứa clorua đặc biệt.
- Nhược điểm: Không phải tất cả các hợp chất chứa clorua đều có thể bị thủy phân để tạo ra HCl.
Lưu ý khi thực hiện:
- An toàn: HCl là chất có tính ăn mòn mạnh, nên tiến hành thí nghiệm trong tủ hút. Đeo kính và găng tay bảo vệ.
- Thiết bị: Sử dụng ngòi nổ để thu khí HCl.
- Khí độc: Khí HCl rất độc, cần thu khí vào ống nghiệm úp ngược để khí nặng hơn không khí chìm xuống đáy ống nghiệm.
Cách chọn phương pháp tạo HCl thích hợp
Để lựa chọn phương pháp tạo axit HCl phù hợp cần căn cứ vào các yếu tố sau:
- Quy mô sản xuất: Sản xuất lớn thường ưu tiên phương pháp tổng hợp trực tiếp.
- Độ tinh khiết cần thiết: Nếu yêu cầu HCl có độ tinh khiết cao. Phương pháp tổng hợp trực tiếp là phù hợp nhất.
- Nguồn nguyên liệu: Nếu có sẵn muối ăn và axit sulfuric. Phương pháp thứ hai có thể được xem xét.
- Sản phẩm đi kèm: Nếu cần sản xuất NaOH và clo cùng lúc. Quá trình chloralkali là một lựa chọn tốt.
Ứng dụng của axit HCl trong đời sống là gì?
Axit clohydric (HCl), còn được gọi là axit muriatic. Nó là một hợp chất hóa học cực kỳ quan trọng và được sử dụng rộng rãi trong nhiều ngành công nghiệp. Với tính axit mạnh và khả năng phản ứng cao. HCl đóng vai trò quan trọng trong nhiều quá trình sản xuất, chế biến. Các ứng dụng chính của HCl bao gồm:
Sản xuất hóa chất:
- Tổng hợp hữu cơ: HCl được sử dụng để sản xuất các hợp chất hữu cơ. Chẳng hạn như vinyl clorua (nguyên liệu chính để sản xuất PVC), dichloromethane và các hợp chất hữu cơ khác.
- Sản xuất muối: HCl phản ứng với bazơ tạo thành muối clorua. Chẳng hạn như natri clorua (muối ăn), canxi clorua, magiê clorua.
- Sản xuất hóa chất khác: HCl được dùng để sản xuất các loại hóa chất khác. Chẳng hạn như axit sulfuric, axit photphoric và các hợp chất clo khác.
Xử lý bề mặt kim loại:
- Loại bỏ rỉ sét: HCl được sử dụng để loại bỏ rỉ sét trên bề mặt kim loại trước khi sơn hoặc mạ.
- Làm sạch kim loại: HCl giúp loại bỏ tạp chất, chất bẩn trên bề mặt kim loại. Tạo điều kiện thuận lợi cho quá trình gia công tiếp theo.
 Hiệu quả tẩy gỉ của dung dịch HCl
Hiệu quả tẩy gỉ của dung dịch HCl
Công nghiệp thực phẩm:
- Điều chỉnh pH: HCl được dùng để điều chỉnh pH trong quá trình sản xuất thực phẩm, đồ uống.
- Sản xuất gelatin: HCl được dùng để tách collagen ra khỏi da động vật trong quá trình sản xuất gelatin.
Ngành dầu khí:
- Kích hoạt giếng dầu: HCl được bơm vào giếng dầu để hòa tan các lớp đá vôi. Tạo vết nứt và tăng khả năng khai thác dầu.
- Xử lý axit: HCl được sử dụng để xử lý axit trong quá trình khai thác và tinh chế dầu.
Xử lý nước:
- Điều chỉnh pH: HCl được dùng để điều chỉnh pH của nước thải công nghiệp trước khi thải ra môi trường.
- Loại bỏ ion kim loại nặng: HCl có thể phản ứng với một số ion kim loại nặng. Tạo thành các hợp chất không hòa tan và dễ dàng loại bỏ.
Ngành dược phẩm:
- Sản xuất dược phẩm: HCl được sử dụng trong sản xuất nhiều loại thuốc.
Ngành xây dựng:
- Sản xuất bê tông: HCl được dùng để điều chỉnh độ pH của bê tông.
- Làm sạch gạch: HCl được dùng để làm sạch các vết bẩn trên gạch và bề mặt xây dựng.
Tham khảo thêm bài viết khác: >>> Hóa chất Axit HCl 32% (Hydrochloric Acid) dùng để vệ sinh bể bơi
Nhà cung cấp axit HCl uy tín trên toàn quốc
Vũ Hoàng là một trong những nhà cung cấp axit HCl uy tín và chất lượng hàng đầu tại Việt Nam. Với kinh nghiệm nhiều năm trong lĩnh vực hóa chất. Vũ Hoàng đã khẳng định được vị thế của mình trên thị trường và được nhiều khách hàng tin tưởng, lựa chọn.
Vũ Hoàng cam kết mang đến cho khách hàng những sản phẩm và dịch vụ tốt nhất!
Từ những thông tin trên, chúng ta có thể thấy axit clohiđric HCl có vai trò vô cùng quan trọng trong nhiều lĩnh vực khác nhau. Từ sản xuất công nghiệp đến nghiên cứu khoa học. Các phương pháp điều chế HCl tuy đa dạng nhưng đều có những ưu điểm và hạn chế riêng.
Việc hiểu rõ tính chất và phương pháp sản xuất HCl không chỉ giúp chúng ta sử dụng hợp chất này một cách hiệu quả. Mà còn bảo vệ sức khỏe và môi trường khi làm việc với hóa chất này. Vì vậy, nắm vững kiến thức về cách tạo ra HCl quan trọng hơn bao giờ hết trong bối cảnh công nghiệp ngày nay.
Hãy theo dõi chúng tôi qua HOTLINE hoặc Website: https://vuhoangco.com.vn để biết thêm thông tin hữu ích.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn