Nội dung bài viết
NaClO là muối natri màu trắng, tồn tại ở dạng tinh thể khan, tên đầy đủ là Natri hypoclorit, có tính ứng dụng cao. Natri hypochlorite được sử dụng trong nhiều ngành sản xuất cũng như lĩnh vực đời sống. Trong bài viết dưới đây vietchem sẽ chia sẻ thông tin chi tiết về NaClO đến các bạn.
1. NaClO (Sodium Hypochlorite) là gì?
Naclo là gì? Natri hypoclorit (NaClO) trong một số trường hợp còn được gọi là Natri clorat, là một hợp chất muối natri. Ở dạng tinh thể, nó có màu trắng, nhưng đôi khi cũng có thể xuất hiện dưới dạng chất lỏng màu vàng nhạt. Ngày nay, Natri Hypochlorite đóng vai trò quan trọng trong sản xuất của nhiều ngành công nghiệp quan trọng, phục vụ nhu cầu sinh hoạt của con người.
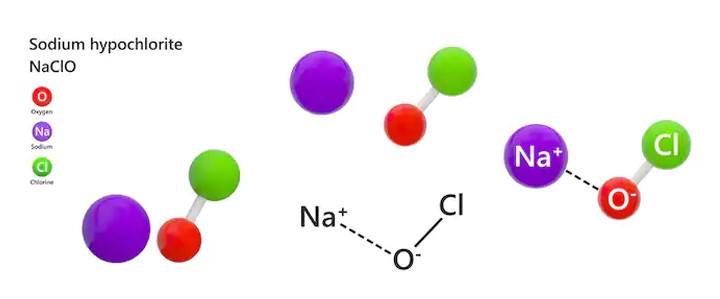
Hình 1: Natri hypoclorit (NaClO)
Cấu trúc phân tử của NaClO bao gồm: cation Natri (Na+) và anion Hypochlorite (OCl hoặc ClO-).
2. Tính chất lý hóa của NaClO
Natri hypochlorite là một hợp chất muối có đặc tính hóa lý độc đáo và hấp dẫn. Hãy cùng Vietchem khám phá tính chất vật lý và hóa học của NaClO:
2.1. Tính chất vật lý của Natri Hypochlorite
NaClO có nhiều tính chất vật lý điển hình, trong đó có những biểu hiện đáng chú ý sau:
- NaClO tồn tại dưới dạng tinh thể màu trắng, có mùi đặc trưng, dễ tan trong nước.
- Độ hòa tan của NaClO trong nước là 29,3 g/100ml.
- Điểm nóng chảy của natri hypoclorit khi ngậm nước là 18 độ C.
- Mật độ của NaClO là 1,11 g/cm3.
- Điểm sôi của natri hypoclorit là 101 độ C.

Hình 2: Natri Hypochlorite là hợp chất muối có đặc tính hóa lý độc đáo
2.2. Tính chất hóa học của Natri Hypochlorite
NaClO thực chất là một trong những hợp chất có đầy đủ các biểu hiện và tính chất hóa học của muối. Điều này được minh họa bằng các phản ứng hóa học sau:
Phản ứng với kim loại tạo thành oxit và muối:
- NaClO + Zn → ZnO + NaCl
Phản ứng với axit clohiđric tạo ra khí clo, nước và muối clorua:
- HCl + NaClO → NaCl + Cl2 + H2O
Phản ứng với một số axit khác, chẳng hạn như axit axetic, để tạo thành axit hypochlorous:
- NaClO + CH3COOH → HClO + CH3COONa
Trong điều kiện nhiệt độ thích hợp, natri hypoclorit phân hủy thành natri clorat và natri clorua:
- 3NaClO → NaClO3 + 2 NaCl
3. Phương pháp điều chế NaClO (Natri hypoclorit)
Hiện nay, có hai phương pháp chính được sử dụng để điều chế Natri Hypochlorite: phương pháp công nghiệp và phương pháp phòng thí nghiệm.
3.1. Phương pháp công nghiệp điều chế NaClO
Trong các quy trình công nghiệp, Natri Hypochlorite thường được sản xuất thông qua quá trình điện phân sử dụng màng. Quá trình này bao gồm việc đưa khí clo vào dung dịch NaOH loãng, lạnh qua màng. Để đảm bảo hiệu suất quá trình, dung dịch luôn được duy trì ở nhiệt độ dưới 40 độ C để tránh hình thành Natri Clorat.
Một phản ứng điển hình trong quá trình này có thể được biểu diễn bằng công thức sau:
- Cl2 + 2 NaOH → NaClO + NaCl + H2O

Hình 3: Các phương pháp điều chế NaClO (Sodium Hypochlorite)
3.2. Điều chế NaClO trong phòng thí nghiệm
Trong phòng thí nghiệm, để điều chế NaClO người ta thường sử dụng phương pháp điện phân dung dịch Natri Clorua trong nước mà không cần dùng màng. Sau đó cho dung dịch này phản ứng với NaCl. Các phản ứng hóa học sẽ diễn ra theo trình tự sau:
- H2O + NaCl ⟶ H2 +NaClO.
- Na2CO3 + Ca(ClO)2 ⟶ CaCO3 + 2NaClO.
- 2 NaOH + NO2Cl ⟶ H2O + NaClO + NaNO2.
- NaOH + HClO ⟶ H2O + NaClO
4. Ứng dụng đa dạng của NaClO trong đời sống
NaClO được sử dụng rộng rãi, phục vụ trực tiếp cho nhu cầu sinh hoạt của gia đình. Đây cũng là nguyên liệu chính trong sản xuất của một số ngành công nghiệp quan trọng.
4.1. NaClO phục vụ cuộc sống gia đình
Natri hypochlorite thường được sử dụng trong gia đình để loại bỏ vết bẩn trên quần áo một cách hiệu quả, đặc biệt là trên vải cotton. Tuy nhiên, phương pháp này có nhược điểm là làm giảm dần chất lượng vải (đặc biệt là cotton), làm giảm tuổi thọ của quần áo. Vì vậy, NaClO thường chỉ được sử dụng để làm sạch những vùng bẩn và không nên dùng để ngâm, tẩy toàn bộ quần áo, vải vóc.
4.2. Ứng dụng NaClO trong y học
Ứng dụng của Natri Hypochlorite trong y học rất rõ ràng, đặc biệt trong quá trình phẫu thuật nha khoa và điều trị tủy răng. Ở đây, NaClO đóng vai trò như một liều thuốc hỗ trợ đắc lực trước khi tổn thương tủy răng xuất hiện.

Hình 4: Ứng dụng đa dạng của NaClO trong đời sống
4.3. Ứng dụng NaClO trong công nghiệp
Natri Hypochlorite là thành phần quan trọng trong việc sản xuất dung dịch tẩy rửa trong quá trình sản xuất bia hoặc rượu, giúp hạn chế mùi hôi trong quá trình ủ bia.
Đặc biệt, dung dịch NaClO loãng còn có tác dụng diệt một số loại vi khuẩn, virus, thường được sử dụng làm chất tẩy rửa, tẩy rửa ở những khu vực bị ô nhiễm như nhà máy, bệnh viện, nhà ăn,….
Ngoài ra, NaClO còn được sử dụng để khử trùng giếng và hệ thống nước uống hiệu quả, làm giảm sự phát triển của vi khuẩn, virus có hại.
Ngoài ra, Natri Hypochlorite thường được sử dụng trong quá trình khử trùng nước uống. Tuy nhiên, quá trình này cần phải được thực hiện cẩn thận và đảm bảo đúng liều lượng vì NaClO có thể ăn mòn và gây hại cho cơ thể nếu sử dụng sai liều lượng.
Ngoài ra, do NaClO có tính kiềm, pH bằng 11 nên dung dịch này còn được dùng để xử lý các loại nước thải có tính loãng như nước thải từ các xưởng mạ điện.
4.4. Ứng dụng Natri Hypochlorite trong thí nghiệm oxy hóa
Khi dung dịch Natri hypoclorit tiếp xúc với chất xúc tác chuyển pha (hay còn gọi là chất xúc tác chuyển pha). Thông qua quá trình oxy hóa rượu sẽ tạo ra các hợp chất cacbonyl.
Trường Chu Văn An vừa chia sẻ thông tin về NaClO (Sodium Hypochlorite) tới các bạn qua nội dung bài viết. Hy vọng bài viết của Vietchem đã mang đến những thông tin hữu ích cho các bạn.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn