Nội dung bài viết
Nitơ là một trong những nguyên tố hóa học có vai trò quan trọng đối với cơ thể con người và sự sống trên trái đất. Vậy nitơ là gì? Giá trị hóa học của nitơ là gì, tính chất và ứng dụng của nó là gì? Trường Chu Văn An sẽ phân tích chi tiết trong bài viết dưới đây.
1. Nitơ là gì?
Nitơ được viết theo công thức hóa học N2. Đây là thành phần chiếm tỷ lệ lớn trong khí quyển và có vai trò quan trọng trong cơ thể sống. Nitơ tham gia vào quá trình bảo vệ trái đất khỏi bức xạ mặt trời.
Hiện nay Nitơ tồn tại ở hai dạng: Nitơ lỏng và Nitơ khí. Đặc biệt, nitơ lỏng có nhiều đặc tính hữu ích nên được sử dụng rộng rãi.
Nitơ tồn tại ở dạng tự do và dạng hợp chất trong tự nhiên. Ở dạng tự do, chúng chiếm tỷ lệ khá cao trong thể tích không khí. Khi tồn tại ở dạng hợp chất, Nitơ là thành phần của nhiều hợp chất như axit nucleic, protein…
Công thức hóa học của Nitơ là N2
2. Hóa trị của nitơ là gì?
Không giống như một số loại khí khác chỉ có một hóa trị duy nhất. Nitơ có 3 hóa trị khác nhau. Bao gồm: Hóa trị II, Hóa trị III và Hóa trị IV.
4. Tính chất của Nitơ
4.1. Tính chất vật lý
Nitơ là chất khí nhẹ hơn không khí, không mùi, không vị, không màu. Chúng ít tan trong nước và đông đặc ở nhiệt độ rất thấp. Nhiệt độ hóa lỏng của Nitơ khoảng -1960C.
Một số thông tin khác về Nitơ:
- Ký hiệu nguyên tử: N
- Số nguyên tử: Số 7 thuộc nhóm VA
- Số oxh của N2: -3, 0, +1, +2, +3, +4, +5
- Nhiệt độ sôi: 77,36K
- Nhiệt độ nóng chảy: 63,15K

Nitơ là chất khí, nhẹ hơn không khí
4.2. Tính chất hóa học
Ngoài việc tìm hiểu về hóa trị của Nitơ, việc hiểu được tính chất hóa học của loại khí này sẽ giúp ích rất nhiều. Theo đó, Nitơ có nhiều số oxi hóa khác nhau trong đó có số 0. Vì vậy, chúng vừa có tính khử, vừa có tính oxi hóa. Nitơ hoạt động mạnh hơn ở nhiệt độ cao nhưng trơ về mặt hóa học trong điều kiện nhiệt độ bình thường.
Tính chất khử của Nitơ
- Nitơ phản ứng với các nguyên tố có độ âm điện lớn hơn do tính chất khử của nó. Đặc biệt ở nhiệt độ cao hơn 30000C. Khi kết thúc phản ứng sẽ thu được Nitơ monoxit.
Phương trình phản ứng: N2 + O2 → 2NO (không màu)
Trong đó, N2 có hóa trị 0, N trong NO có hóa trị +2.
- Ở điều kiện nhiệt độ bình thường, Nitơ monoxit sẽ phản ứng với oxy trong không khí. Kết quả là nitơ dioxide có màu nâu đỏ.
Phương trình phản ứng: 2NO + O2 → 2NO2
Đặc biệt, N trong NO2 có hóa trị +4.
Tính chất oxy hóa của nitơ
Nitơ phản ứng với các nguyên tố có độ âm điện ít hơn do tính chất oxy hóa của nó. Bao gồm các phản ứng với kim loại và hydro:
- Phản ứng với kim loại
Trong điều kiện bình thường: Nitơ chỉ phản ứng với Li tạo thành Lithium Nitride.
Phương trình: 6Li + N2 → 2Li3N
Trong điều kiện nhiệt độ cao, Nitơ có thể phản ứng với nhiều kim loại khác nhau tạo thành Nitride. Tuy nhiên, Nitride dễ bị thủy phân tạo thành NH3.
Phương trình: 3Mg + N2 → Mg3N2
- Phản ứng với hydro
Nitơ phản ứng với hydro ở nhiệt độ và áp suất cao bằng chất xúc tác. Khi kết thúc phản ứng, amoniac được hình thành.
Phương trình phản ứng: N2 + 3H2 ↔ 2NH3
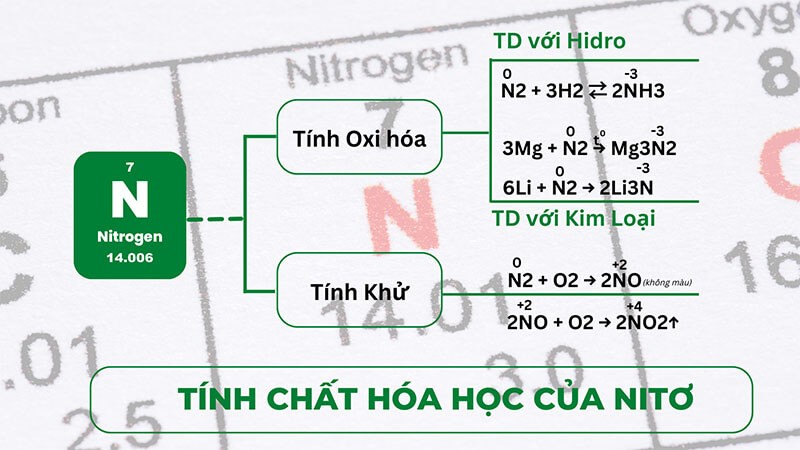
Tính chất hóa học của nitơ
5. Ứng dụng Nitơ
Khả năng ứng dụng của Nitơ và Nitơ hóa trị đã được nghiên cứu khá nhiều. Hiện nay, khí nitơ được sử dụng rộng rãi trong đời sống. Bao gồm:
- Trong nghiên cứu giáo dục: Phân tích mẫu và sử dụng để nghiên cứu các hợp chất hóa học.
- Trong chế biến sinh học và vận chuyển thực phẩm: Nitơ đóng vai trò làm lạnh đảm bảo an toàn trong bảo quản thực phẩm.
- Trong y học: Bảo vệ các bộ phận cơ thể khỏi bị phân hủy. Đặc biệt là bảo quản trứng và tinh trùng trong quá trình vận chuyển.
- Trong gia công và luyện kim kim loại: Nguyên liệu trong sản xuất thép không gỉ, linh kiện điện tử, luyện kim…
- Trong sản xuất lốp máy bay và ô tô: Bơm lốp ô tô và bơm lốp máy bay.
- Trong gia công kim loại và hàn ống: Làm sạch đường ống, giúp giảm thiểu hư hỏng trong quá trình sử dụng thiết bị.
- Trong bảo quản thực phẩm: Nitơ có tính trơ nên có khả năng ngăn chặn quá trình oxy hóa tốt. Vì vậy, sử dụng Nitơ để bảo quản thực phẩm là một trong những biện pháp hữu ích.
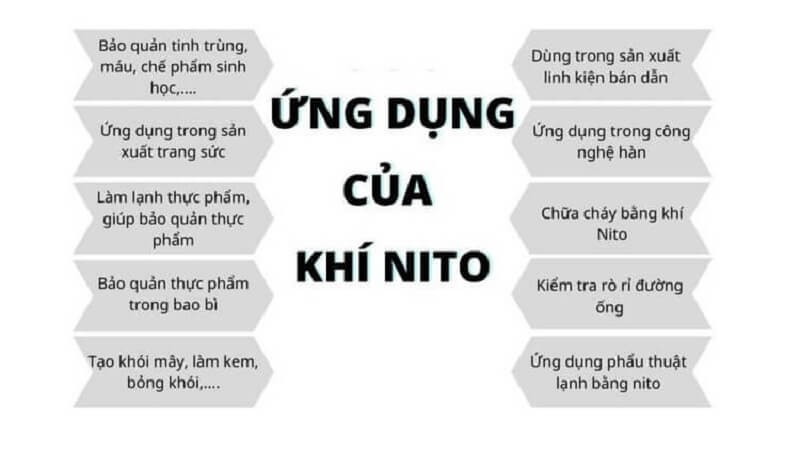
Nitơ có nhiều ứng dụng trong đời sống
6. Cách điều chế Nitơ
Trong phòng thí nghiệm
Sử dụng dung dịch muối amoni nitrit bão hòa để điều chế nitơ là phương pháp phổ biến trong phòng thí nghiệm.
Trong công nghiệp
Điều chế nitơ trong công nghiệp bằng cách chưng cất phân đoạn không khí lỏng. Nitơ thu được ở nhiệt độ -1960C và được bảo quản trong thùng thép nén có áp suất 125at.
Hoá trị của nitơ đã được chia sẻ chi tiết ở bài viết trên. Hy vọng những chia sẻ của Trường Chu Văn An sẽ giúp giải đáp mọi thắc mắc của bạn. Nếu bạn có nhu cầu tìm hiểu thêm hãy liên hệ với chúng tôi theo số hotline để được hỗ trợ.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn